
题目列表(包括答案和解析)

图4-19
(1)a电极材料应为_________;b电极材料为________。b电极的电极反应式为_______。
(2)电解液c可以是(填编号)__________________。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为_______________,在加入苯之前,对c溶液应作何简单处理?
(4)为了在较短时间内看到白色沉淀,可采取的措施有____________。
A.改用稀硫酸作电解液 B.适当增大电源的电压
C.适当减小两电极间的距离 D.适当降低电解液的浓度

(1)a电极材料应为 ,电极反应式为 。
(2)电解液c可以是(填编号) 。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为一苯层,其作用为 ,在加入苯之前对c应作何简单处理? 。
(4)若c中用Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象是 。
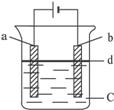
图6-28
(1)a电极材料应为____________,电极反应式为_________________。
(2)电解液C可以(填编号)是_____________。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用是___________,在加入苯之前对C应作何简单处理________________。
(4)为了在较短时间内看到白色沉淀,可采取的措施是(填编号)___________。
A.改用稀硫酸作电解液 B.适当增大电源的电压
C.适当减小两电极间的距离 D.适当降低电解液的温度
(5)若C中用Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一现象是_______________________________。

(1)a电极材料应为____________,b电极的电极反应式为______________。
(2)电解液c可以是____________(填编号)。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)d为苯,其作用为________________________,在加入苯之前,对c溶液应做简单处理____________________________________________________________。
(4)为了在较短时间内看到白色沉淀,可采取的措施是____________(填编号)。
A.改用稀硫酸作电解液 B.适当增大电源的电压
C.适当减小两电极间的距离 D.适当降低电解液的浓度

图1-10
(1)a电极材料应为什么材料?
(2)电解液c可以是什么溶液?
(3)d为苯,其作用为隔开空气,防止生成的Fe(OH)2被氧化生成Fe(OH)3,在加苯之前,对c溶液应作何简单处理?
(4)为了在较短时间内看到白色沉淀,可采取哪些措施?
(5)你能否根据图中的仪器装置而不添加任何仪器制得Fe(OH)3?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com