
题目列表(包括答案和解析)
I.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合韧是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 ;
(2)液氨是富氢物质,是氢能的理想载体,利用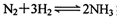 实现储氢和输氢。下列说法正确的是
;
实现储氢和输氢。下列说法正确的是
;
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH+4与PH+4、CH4、BH-4、ClO—4互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+离子中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是 ;
II.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。
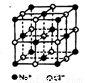
(1)设氯化钠晶体中Na+与跟它最近邻的Cl—之间的距离为r,则该Na+与跟它次近邻的C1—个数为 ,该Na+与跟它次近邻的Cl—之间的距离为 ;
(2)已知在氯化钠晶体中Na+的半径为以a pm,Cl—的半径为b pm,它们在晶
体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为 ;(用含a、b的式子袁示)
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为 。

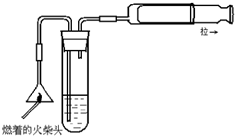 火柴头中含有硫和氯元素,用适当的方法可加以检验,回答下列问题:
火柴头中含有硫和氯元素,用适当的方法可加以检验,回答下列问题: (选做题)
(选做题)| 45V |
| 28 |
| 45V |
| 28 |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com