
题目列表(包括答案和解析)
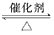 2SO3,平衡时SO3为a mol,在相同温度下分别按下列配比在V L密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是
2SO3,平衡时SO3为a mol,在相同温度下分别按下列配比在V L密闭容器中放入起始物质,平衡时有关SO3的物质的量叙述正确的是 2SO3;如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2
2SO3;如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是_____________;bc过程中改变的条件可能是_____________; 若增大压强时,反应速度变化情况画在c-d处
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是_____________;bc过程中改变的条件可能是_____________; 若增大压强时,反应速度变化情况画在c-d处

(10分)一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O22SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1) 反应5min内,v(O2)=_________mol.L-1.min-1.
(2) 化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3) 判断该反应达到平衡的标志是_______________;
A.v消耗(SO2)=v生成(SO3) B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变 D.容器中气体的总物质的量不再变化
(10分)一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O2 2SO3.5min后达到平衡,测得容器中有SO31.6mol.
2SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1) 反应5min内,v(O2)=_________mol.L-1.min-1.
(2) 化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3) 判断该反应达到平衡的标志是_______________;
| A.v消耗(SO2)=v生成(SO3) | B.混合气体的平均相对分子质量不再改变 |
| C.混合气体的密度不再改变 | D.容器中气体的总物质的量不再变化 |
(10分)一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O2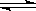 2SO3.5min后达到平衡,测得容器中有SO31.6mol.
2SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1) 反应5min内,v(O2)=_________mol.L-1.min-1.
(2) 化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3) 判断该反应达到平衡的标志是_______________;
A.v消耗(SO2)=v生成(SO3) B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变 D.容器中气体的总物质的量不再变化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com