
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ОЇЬхОпгаЙцдђЕФМИКЮЭтаЮЃЌОЇЬхжазюЛљБОЕФжиИДЕЅдЊГЦЮЊОЇАћЁЃNaClОЇЬхНсЙЙШчЭМЫљЪОЁЃвбжЊFexOОЇЬхОЇАћНсЙЙЮЊNaClаЭЃЌгЩгкОЇЬхШБЯнЃЌxжЕаЁгк1ЁЃВтжЊFexOОЇЬхУмЖШІбЮЊ5.71g/cm3ЃЌОЇАћБпГЄЮЊ4.28ЁС10Ѓ10mЁЃЃЈЬњЯрЖддзгжЪСПЮЊ55.9ЃЌбѕЯрЖддзгжЪСПЮЊ16ЃЉЧѓЃК
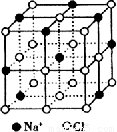
ЃЈ1ЃЉFexOжаxжЕЃЈОЋШЗжС0.01ЃЉЮЊ_____________ЁЃ
ЃЈ2ЃЉОЇЬхжаЕФFeЗжБ№ЮЊFe2ЃЋЁЂFe3ЃЋЃЌдкFe2ЃЋКЭFe3ЃЋЕФзмЪ§жаЃЌFe2ЃЋЫљеМЗжЪ§ЃЈгУаЁЪ§БэЪОЃЌОЋШЗжС0.001ЃЉЮЊ___________ЁЃ
ЃЈ3ЃЉДЫОЇЬхЛЏбЇЪНЮЊ___________ЁЃ
ЃЈ4ЃЉFeдкДЫОЇЬхжаеМОнПеЯЖЕФМИКЮаЮзДЪЧ___________ЃЈМДгыO2ЃОрРызюНќЧвЕШОрРыЕФЬњРызгЮЇГЩЕФПеМфаЮзДЃЉЁЃ
ЃЈ5ЃЉдкОЇЬхжаЃЌЬњдЊЫиЕФРызгМфзюЖЬОрРыЮЊ________mЁЃ
ОЇЬхОпгаЙцдђЕФМИКЮЭтаЮЃЌОЇЬхжазюЛљБОЕФжиИДЕЅдЊГЦЮЊОЇАћЁЃNaClОЇЬхНсЙЙШчЭМЫљЪОЁЃвбжЊFexOОЇЬхОЇАћНсЙЙЮЊNaClаЭЃЌгЩгкОЇЬхШБЯнЃЌxжЕаЁгк1ЁЃВтжЊFexOОЇЬхУмЖШІбЮЊ5.71g/cm3ЃЌОЇАћБпГЄЮЊ4.28ЁС10Ѓ10mЁЃЃЈЬњЯрЖддзгжЪСПЮЊ55.9ЃЌбѕЯрЖддзгжЪСПЮЊ16ЃЉЧѓЃК
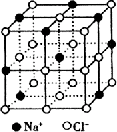
ЃЈ1ЃЉFexOжаxжЕЃЈОЋШЗжС0.01ЃЉЮЊ_____________ЁЃ
ЃЈ2ЃЉОЇЬхжаЕФFeЗжБ№ЮЊFe2ЃЋЁЂFe3ЃЋЃЌдкFe2ЃЋКЭFe3ЃЋЕФзмЪ§жаЃЌFe2ЃЋЫљеМЗжЪ§ЃЈгУаЁЪ§БэЪОЃЌОЋШЗжС0.001ЃЉЮЊ___________ЁЃ
ЃЈ3ЃЉДЫОЇЬхЛЏбЇЪНЮЊ___________ЁЃ
ЃЈ4ЃЉFeдкДЫОЇЬхжаеМОнПеЯЖЕФМИКЮаЮзДЪЧ___________ЃЈМДгыO2ЃОрРызюНќЧвЕШОрРыЕФЬњРызгЮЇГЩЕФПеМфаЮзДЃЉЁЃ
ЃЈ5ЃЉдкОЇЬхжаЃЌЬњдЊЫиЕФРызгМфзюЖЬОрРыЮЊ________mЁЃ
ФГаЃЛЏбЇаЁзщбЇЩњРћгУЯТЭМЫљСазАжУНјааЁАЬњгыЫЎЗДгІЁБЕФЪЕбщЃЌВЂРћгУВњЮяНјвЛВНжЦШЁFeCl3ЁЄ6H2OОЇЬхЁЃЃЈЭМжаМаГжМАЮВЦјДІРэзАжУОљвбТдШЅЃЉ
ЃЈ1ЃЉзАжУBжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЁЃ
ЃЈ2ЃЉзАжУEжаЕФЯжЯѓЪЧ ЁЃ
ЃЈ3ЃЉЭЃжЙЗДгІЃЌД§BЙмРфШДКѓЃЌШЁЦфжаЕФЙЬЬхЃЌМгШыЙ§СПЯЁбЮЫсГфЗжЗДгІЃЌЙ§ТЫЁЃНЋТЫвКЗжГЩСНЗнЃЌЗжБ№МьбщТЫвКжаЕФН№ЪєбєРызгЁЃМьбщFe3ЃЋЫљгУЪдМСЮЊ ЃЌМьбщFe2ЃЋЫљгУЪдМСЮЊ ЁЃ
ЃЈ4ЃЉИУаЁзщбЇЩњРћгУЩЯЪіТЫвКжЦШЁFeCl3ЁЄ6H2OОЇЬхЃЌЩшМЦСїГЬШчЯТЃК
ЂйВНжшвЛжаЭЈШызуСПCl2ЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ ЁЃ
ЂкВНжшЖўДгFeCl3ЯЁШмвКжаЕУЕНFeCl3ЁЄ6H2OОЇЬхЕФжївЊВйзїШчЯТЃЈОљдкHClЦјЗежаНјааЃЉЃК
еєЗЂЁЂХЈЫѕ Ёњ РфШДЁЂНсОЇ Ёњ Й§ТЫЁЂЯДЕгЁЂИЩдя
дкеєЗЂУѓжаНјааеєЗЂХЈЫѕВйзїЪБЃЌЕБ_________________________ЪБЃЌгІЭЃжЙМгШШЁЃДЫЙ§ГЬгІБЃГжбЮЫсЙ§СПЕФдвђ________________________________________ЃЈгУРызгЗНГЬЪНБэЪОЃЉЁЃ
ЃЈ5ЃЉFeCl3ШмвКПЩгУгкЬьШЛЦјЭбСђЃЌаДFeCl3ШмвКгыЬьШЛЦјжаH2SЗДгІЕФРызгЗНГЬЪНЃК ЁЃ
ЃЈ13ЗжЃЉФГаЃЛЏбЇаЁзщбЇЩњРћгУЯТЭМЫљСазАжУНјааЁАЬњгыЫЎЗДгІЁБЕФЪЕбщЃЌВЂРћгУВњЮяНјвЛВНжЦШЁFeCl3ЁЄ6H2OОЇЬхЁЃЃЈЭМжаМаГжМАЮВЦјДІРэзАжУОљвбТдШЅЃЉ
ЃЈ1ЃЉзАжУBжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЃЛ
ЃЈ2ЃЉзАжУEжаЕФЯжЯѓЪЧ ЁЃ
ЃЈ3ЃЉЭЃжЙЗДгІЃЌД§BЙмРфШДКѓЃЌШЁЦфжаЕФЙЬЬхЃЌМгШыЙ§СПЯЁбЮЫсГфЗжЗДгІЃЌЙ§ТЫЁЃНЋТЫвКЗжГЩСНЗнЃЌЗжБ№МьбщТЫвКжаЕФН№ЪєбєРызгЁЃМьбщFe3ЃЋЫљгУЪдМСЮЊ ЃЌМьбщFe2ЃЋЫљгУЪдМСЮЊ ЁЃ
ЃЈ4ЃЉИУаЁзщбЇЩњРћгУЩЯЪіТЫвКжЦШЁFeCl3ЁЄ6H2OОЇЬхЃЌЩшМЦСїГЬШчЯТЃК
ЂйВНжшвЛжаЭЈШызуСПCl2ЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ ЁЃ
ЂкВНжшЖўДгFeCl3ЯЁШмвКжаЕУЕНFeCl3ЁЄ6H2OОЇЬхЕФжївЊВйзїШчЯТЃЈОљдкHClЦјЗежаНјааЃЉЃК
еєЗЂЁЂХЈЫѕ Ёњ РфШДЁЂНсОЇ Ёњ Й§ТЫЁЂЯДЕгЁЂИЩдя
дкеєЗЂУѓжаНјааеєЗЂХЈЫѕВйзїЪБЃЌЕБ_________________________ЪБЃЌгІЭЃжЙМгШШЁЃДЫЙ§ГЬгІБЃГжбЮЫсЙ§СПЕФдвђ________________________________________ЃЈгУРызгЗНГЬЪНБэЪОЃЉЁЃ
ФГаЃЛЏбЇаЁзщбЇЩњРћгУЯТЭМЫљСазАжУНјааЁАЬњгыЫЎЗДгІЁБЕФЪЕбщЃЌВЂРћгУВњЮяНјвЛВНжЦШЁFeCl3ЁЄ6H2OОЇЬхЁЃЃЈЭМжаМаГжМАЮВЦјДІРэзАжУОљвбТдШЅЃЉ
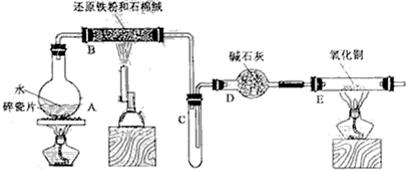
ЃЈ1ЃЉзАжУBжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЁЃ
ЃЈ2ЃЉзАжУEжаЕФЯжЯѓЪЧ ЁЃ
ЃЈ3ЃЉЭЃжЙЗДгІЃЌД§BЙмРфШДКѓЃЌШЁЦфжаЕФЙЬЬхЃЌМгШыЙ§СПЯЁбЮЫсГфЗжЗДгІЃЌЙ§ТЫЁЃНЋТЫвКЗжГЩСНЗнЃЌЗжБ№МьбщТЫвКжаЕФН№ЪєбєРызгЁЃМьбщFe3ЃЋЫљгУЪдМСЮЊ ЃЌМьбщFe2ЃЋЫљгУЪдМСЮЊ ЁЃ
ЃЈ4ЃЉИУаЁзщбЇЩњРћгУЩЯЪіТЫвКжЦШЁFeCl3ЁЄ6H2OОЇЬхЃЌЩшМЦСїГЬШчЯТЃК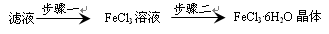
ЂйВНжшвЛжаЭЈШызуСПCl2ЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ ЁЃ
ЂкВНжшЖўДгFeCl3ЯЁШмвКжаЕУЕНFeCl3ЁЄ6H2OОЇЬхЕФжївЊВйзїШчЯТЃЈОљдкHClЦјЗежаНјааЃЉЃК
еєЗЂЁЂХЈЫѕ Ёњ РфШДЁЂНсОЇ Ёњ Й§ТЫЁЂЯДЕгЁЂИЩдя
дкеєЗЂУѓжаНјааеєЗЂХЈЫѕВйзїЪБЃЌЕБ_________________________ЪБЃЌгІЭЃжЙМгШШЁЃДЫЙ§ГЬгІБЃГжбЮЫсЙ§СПЕФдвђ________________________________________ЃЈгУРызгЗНГЬЪНБэЪОЃЉЁЃ
ЃЈ5ЃЉFeCl3ШмвКПЩгУгкЬьШЛЦјЭбСђЃЌаДFeCl3ШмвКгыЬьШЛЦјжаH2SЗДгІЕФРызгЗНГЬЪНЃК ЁЃ
вЛЁЂ1.НтЮіЃКXдкЂёAзхЃЌYдЊЫи=5 МД15КХдЊЫиЮЊСзЃЌZдЊЫиЮЊ8КХдЊЫиЃЌМДбѕЁЃПЩзщГЩЃКHPO3ЁЂH3PO4ЁЂH4P2O7
Д№АИЃКA
2.D 3.B 4.D?
5.НтЮіЃКдкРызгЛЏКЯЮяNaOHжаЃЌМШКЌгаРызгМќгжгаЙВМлМќЁЃ
Д№АИЃКC
6.C
7.НтЮіЃКNH4H+H2O===NH3?H2O+H2Ёќ?
Д№АИЃКC?
8.C 9.D
(3) 2Cl2ЃЋ2CaЃЈOHЃЉ2===CaCl2ЃЋCaЃЈClOЃЉ2ЃЋ2H2O?
12.ЙВМл Ш§ е§ЫФУцЬх 60Ёу 6 P4O6?
13.OHЃ NH H2O NH3 H3O+ е§ЫФУцЬх?
14.ЃЈ1ЃЉЧт бѕ Сђ ТС ФЦ УО?
ЃЈ2ЃЉЂйH2S+OHЃ===HSЃ+H2OЛђHSЃ+OHЃ===S2Ѓ+H2O?
ЂкOHЃЃОS2Ѓ(ЛђHSЃ)?
17.ЃЈ1ЃЉx=0.92?
ЃЈ2ЃЉ82.6%?
ЃЈ3ЃЉ19 FeO?2Fe2O3?
ЃЈ4ЃЉ3.03ЁС10Ѓ10m
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com