
题目列表(包括答案和解析)
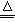 5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。

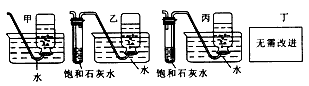
实验室用浓盐酸和二氧化锰制氯气,并用氯气和氢氧化钙反应制少量的漂白粉。现已知反应2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,温度稍高时即发生副反应:6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。有三位同学设计的三套制漂白粉的实验装置如下:
(1)若从下列几个方面对甲、乙、丙三套装置的优缺点作出评价,试选择符合题目要求的选项序号填入下表中。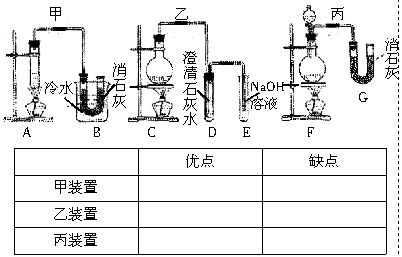
a.不容易控制反应速率
b.容易控制反应速率
c.有副反应发生
d.能防止副反应的发生
e.污染环境
f.可防止污染环境
(2)请从上述甲、乙、丙装置中选择合理的组成部分,组装一套较完善的实验装置,装置的各部分按气流从左至右的连接顺序是(用字母表示)______________
__________________________________。
(3)实验中若取100mL12mol?L-1盐酸与足量二氧化锰反应,最终生成Ca(ClO)2的物质的量总是________(填“大于”、“小于”或“等于”)0.15mol,其可能的原因是(假设各步反应物质无损耗,且无副反应发生)__________________________________________。
工业上以黄铁矿为原料生产硫酸主要分为三个阶段进行,即在沸腾炉中煅烧黄铁矿、SO2的催化氧化及其SO3的吸收。请回答下列几个有关硫酸工业中的几个问题。
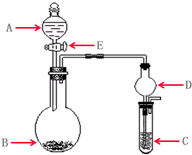
(1)生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧。反应的化学方程式为:2FeSO4·7H2O ![]() Fe2O3 + SO2↑+ SO3↑+ 14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。下列关于该反应说法正确的是( )
Fe2O3 + SO2↑+ SO3↑+ 14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管。下列关于该反应说法正确的是( )

A.若将反应后的三种气体通入BaCl2溶液中,产生的沉淀为BaSO3、BaSO4
B.b中产物用紫色石蕊试液即可检验出其中H+和SO42—
C.为检验反应的另一种生成物,试管c中应加入的试剂为NaOH溶液
D.b中所得到的硫酸的质量分数为29.5%
(2)从沸腾炉中出来的炉气必须经除尘、洗涤、干燥后进入接触室,其主要目的是__________。
(3)接触室中热交换器是实现冷热交换的装置。化学实验中也经常利用热交换来实现某种实验目的,如气、液热交换时通常使用的仪器是______________。
(4)接触室中主要反应是SO2的催化氧化,在生成硫酸的过程中,钒触媒(V2O5)所以能加快二氧化硫氧化的速度,除了具有吸附作用外,有人认为反应过程中还产生了一连串的中间体(如图)。c步的化学方程式可表示为_______________________。

(5) 工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品。将尾气通入粉末状的碳酸钙或熟石灰的悬浊液中,经过一系列处理后得到一种相对分子质量为172的化工原料J。试写出J的化学式_________。
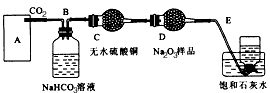
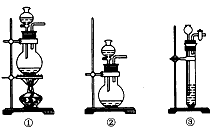
 (2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)
(2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)一、1.解析:液态物质的沸点与压强有关,减小压强,能降低其沸点,这样就能在温度不变的情况下使水蒸发而H2O2又不会分解。?
答案:B?
2.B 3.C 4.A 5.AB 6.B 7.D 8.C 9.BC 10.A?
二、11.(1)氧化 (2)还原?
(3)PbS+4H2O2===PbSO4+4H2O?
12.(1)④ (2)②③ (3)①⑤?
13. g(H2S过量),
g(H2S过量), g(SO2过量)?
g(SO2过量)?
14.(1)
(2)过量铁粉被氧化为氧化物,与酸反应不再产生气体,故产生气体体积小于
15.(1)CS2+Na2S===Na2CS3?
(2)P2S5+K2S===2KPS3?
(3) Na2S2+2HCl===2NaCl+S↓+H2S↑
16.(1)含有SO 或SO
或SO 中的一种,或两种都有。
中的一种,或两种都有。
(2)BaCO3?
(3)Br-、S2-
CO 、HCO
、HCO (除SO
(除SO 或SO
或SO 以外)
以外)
17.(1)A:Na2S B:Na2SO
(2)D中:NaCl 0.1 mol?L-1,HCl 0.1 mol?L-1,H2S 0.02 mol?L-1
F中:NaCl 0.1 mol?L-1,HCl 0.1 mol?L-1
(3)2Na2S+Na2SO3+6HCl===6NaCl+3S↓+3H2O?
2Na2S+4HCl===4NaCl+2H2S
S+O2 SO2?
SO2?
2H2S+SO2===3S↓+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com