
题目列表(包括答案和解析)
| ||
| ||
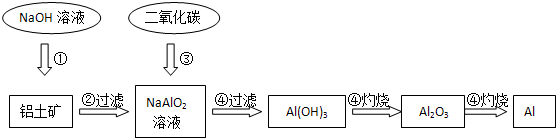
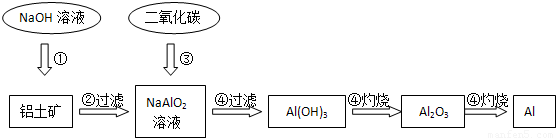
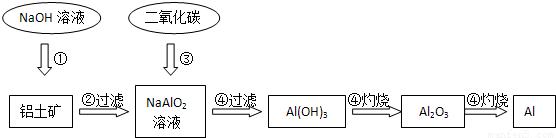
铝土矿(主要成分为Al2O3,还有少量杂质)是提取氧化铝的原料。提取氧化铝的工艺流程如下:
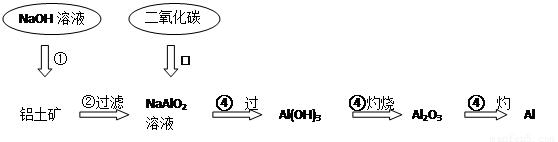
(1)请用离子方程式表示以上工艺流程中第①步反应:_______ _______。
(2)写出以上工艺流程中第③步反应的化学方程式:______ ___________。
(3)金属铝与氧化铁混合在高温下,会发生剧烈的反应。该反应的化学方程式_____________。请举一例该反应的用途________________。
(4)电解熔融氧化铝制取金属铝,若有0.9mol电子发生转移.理论上能得到金属铝的质量是________________。

一、1.BD 2.B 3.D 4.A 5.B 6.AC 7.D 8.AC 9.B?
10.解析:SO2 + 2NaOH===Na2SO3+H2O?
3 mol 6 mol 3 mol?
SO2 + NaOH===NaHSO3?
5 mol 5 mol 5 mol?
故n(SO2)∶n(NaOH)=(3+5)mol∶(6+5)mol=8∶11。?
答案:C
二、11.(1)②③⑤
(2)④
(3)①⑦⑧
(4)②⑤⑦⑧
(5)①
(6)⑥?
12.(1)氯气 二氧化硫?
(2)Cl2+2H2O+SO2===4H++2Cl-+SO
Ag++Cl-===AgCl↓
Ba2++SO ===BaSO4↓?
===BaSO4↓?
13.(1)a h i b c f g d?
(2)作用是使浓硫酸能顺利地滴入烧瓶中;原理是维持烧瓶内压强与分液漏斗内压强相等
(3)先加热V2O5,后缓缓滴入浓硫酸?
(4)有无色(或白色)晶体(或固体)生成?
(5)减小
(6) ×100%或
×100%或 ×100%
×100%
14.(1) (2)
(2) (3)
(3) <b<
<b<
15.(1)4 (2)
16.(1)a= (2)a=
(2)a= (3)
(3)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com