
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
Θ®06Ρξ»ΪΙζΨμ2Θ©Θ®15Ζ÷Θ©“―÷ΣXΓΔYΓΔZΕΦ «ΕΧ÷ήΤΎΒΡ‘ΣΥΊΘ§ΥϋΟ«ΒΡ‘≠Ή”–ρ ΐ“ά¥ΈΒί‘ωΓΘX‘≠Ή”ΒΡΒγΉ”≤ψ ΐ”κΥϋΒΡΚΥΆβΒγΉ”Ήή ΐœύΆ§Θ§ΕχZ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒΡ»ΐ±ΕΘ§YΚΆZΩ…“‘–Έ≥…ΝΫ÷÷“‘…œΤχΧ§Μ·ΚœΈοΘ§‘ρ
Θ®1Θ©X «____ Θ§Y « _____ Θ§Z «_____ΓΘ
Θ®2Θ©”…YΚΆZΉι≥…Θ§«“YΚΆZΒΡ÷ ΝΩ±»ΈΣ7ΘΚ20ΒΡΜ·ΚœΈοΒΡΜ·―ß ΫΘ®Ζ÷Ή” ΫΘ© «_____ ΓΘ
Θ®3Θ©”…XΓΔYΓΔZ÷–ΒΡΝΫ÷÷‘ΣΥΊΉι≥…Θ§«“”κXΓΔZΖ÷Ή”ΨΏ”–œύΆ§ΒγΉ” ΐΒΡΝΫ÷÷άκΉ” «__________ΚΆ _____ ΓΘ
Θ®4Θ©XΓΔYΓΔZΩ…“‘–Έ≥…“Μ÷÷―ΈΘ§¥Υ―Έ÷–XΓΔYΓΔZ‘ΣΥΊΒΡ‘≠Ή”ΒΡΗω ΐ±»ΈΣ423Θ§ΗΟ―ΈΒΡΜ·―ß ΫΘ®Ζ÷Ή” ΫΘ© «____ ΓΘ
Θ®05Ρξ»ΪΙζΨμ2Θ©“―÷ΣΖ¥”ΠA2Θ®gΘ©ΘΪ2B2Θ®gΘ©![]() 2AB2Θ®gΘ©ΒΡΓςHΘΦ0Θ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®Θ©
2AB2Θ®gΘ©ΒΡΓςHΘΦ0Θ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ®Θ©
A. …ΐΗΏΈ¬Ε»Θ§’ΐœρΖ¥”ΠΥΌ¬ ‘ωΦ”Θ§ΡφœρΖ¥”ΠΥΌ¬ Φθ–Γ
B. …ΐΗΏΈ¬Ε»”–άϊ”ΎΖ¥”ΠΥΌ¬ ‘ωΦ”Θ§¥”ΕχΥθΕΧ¥οΒΫΤΫΚβΒΡ ±Φδ
C. ¥οΒΫΤΫΚβΚσΘ§…ΐΗΏΈ¬Ε»Μρ‘ω¥σ―Ι«ΩΕΦ”–άϊ”ΎΗΟΖ¥”ΠΤΫΚβ’ΐœρ“ΤΕ·
D. ¥οΒΫΤΫΚβΚσΘ§ΫΒΒΆΈ¬Ε»ΜρΦθ–Γ―Ι«ΩΕΦ”–άϊ”ΎΗΟΖ¥”ΠΤΫΚβ’ΐœρ“ΤΕ·


| ||
| ||
Θ®16Ζ÷Θ©IΓΔΙΊ”ΎAsΒΡΖ¥”Π÷–Θ§Ζ¥”ΠΈο”κ…ζ≥…Έο”–ΘΚAsH3ΓΔH2SO4ΓΔKBrO3ΓΔK2SO4ΓΔH3AsO4ΓΔH2OΚΆ“Μ÷÷Έ¥÷ΣΈο÷ XΓΘ
ΔΌ“―÷ΣKBrO3‘ΎΖ¥”Π÷–ΒΟΒΫΒγΉ”Θ§‘ρΗΟΖ¥”ΠΒΡΜΙ‘≠ΦΝ « ΓΘ
ΔΎ“―÷Σ0.2molKBrO3‘ΎΖ¥”Π÷–ΒΟΒΫ1molΒγΉ”…ζ≥…XΘ§‘ρXΒΡΜ·―ß ΫΈΣ ΓΘ
ΔέΗυΨί…œ ωΖ¥”ΠΩ…ΆΤ÷Σ ΓΘΘ®Χν–ρΚ≈Θ©
A.―θΜ·–‘ΘΚKBrO3ΘΨH3AsO4 B.―θΜ·–‘ΘΚH3AsO4ΘΨKBrO3
C.ΜΙ‘≠–‘ΘΚAsH3ΘΨX D.ΜΙ‘≠–‘ΘΚXΘΨAsH3
Δή‘ΎΗΟΖ¥”Π÷–Θ§―θΜ·ΦΝ”κΜΙ‘≠ΦΝΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ ΓΘ
ΔρΓΔXΓΔYΓΔZΓΔWΓΔLΓΔMΝυ÷÷ΕΧ÷ήΤΎ÷ςΉε‘ΣΥΊΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–XΓΔMΒΡΒΞ÷ ‘Ύ≥ΘΈ¬œ¬≥ ΤχΧ§Θ§YΒΡ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ «ΤδΒγΉ”≤ψ ΐΒΡ2±ΕΘ§Z‘ΎΆ§÷ήΤΎΒΡ÷ςΉε‘ΣΥΊ÷–‘≠Ή”ΑκΨΕΉν¥σΘ§W «ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡΫπ τ‘ΣΥΊΘ§LΒΡΒΞ÷ ΨßΧε»έΒψΗΏΓΔ”≤Ε»¥σΘ§ «“Μ÷÷÷Ί“ΣΒΡΑκΒΦΧε≤ΡΝœΓΘ”ΟΜ·―ß”Ο”οΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©M‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷ΟΈΣ ΓΘ
Θ®2Θ©YΓΔLΓΔMΒΡΉνΗΏΦέΚ§―θΥαΒΡΥα–‘”…»θΒΫ«ΩΒΡΥ≥–ρ « Θ®–¥Μ·―ß ΫΘ©ΓΘ
Θ®3Θ©‘≠Ή”–ρ ΐ±»YΕύ2ΒΡ‘ΣΥΊΒΡ“Μ÷÷«βΜ·ΈοΡήΖ÷ΫβΈΣΥϋΒΡΝμ“Μ÷÷«βΜ·ΈοΘ§¥ΥΖ÷ΫβΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ « ΓΘ
Θ®4Θ©–¥≥ωZΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·Έο”κΒΞ÷ WΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ
ΓΘ
Θ®5Θ©R”κYΆ§÷ήΤΎΘ§RΒΡΒΞ÷ Ζ÷Ή”R2÷–”–3ΗωΙ≤ΦέΦϋΘ§R”κLΡή–Έ≥…“Μ÷÷–¬–ΆΈόΜζΖ«Ϋπ τ≤ΡΝœΘ§ΤδΜ·―ß Ϋ « ΓΘ
Θ®6Θ©Ββ «»ΥΧε±Ί–ηΒΡΈΔΝΩ‘ΣΥΊ÷°“ΜΘ§”–ΓΑ÷«ΝΠ‘ΣΥΊΓ±÷°≥ΤΓΘΈ“Ιζ¥”1989ΡξΩΣ ΦΘ§÷π≤Ϋ“‘KIO3»Γ¥ζKIΦ”ΙΛΒβ―ΈΓΘ“―÷Σ‘ΎΥα–‘»ή“Κ÷–Ω…ΖΔ…ζΖ¥”ΠΘΚ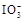 +5I-+6H+=3I2+3H2OΘ§Ψί¥ΥΖ¥”ΠΘ§Ω…”Ο ‘÷ΫΚΆ“Μ–©…ζΜν÷–≥ΘΦϊΒΡΈο÷ …ηΦΤ Β―ιΘ§÷ΛΟς ≥―Έ÷–¥φ‘Ύ
+5I-+6H+=3I2+3H2OΘ§Ψί¥ΥΖ¥”ΠΘ§Ω…”Ο ‘÷ΫΚΆ“Μ–©…ζΜν÷–≥ΘΦϊΒΡΈο÷ …ηΦΤ Β―ιΘ§÷ΛΟς ≥―Έ÷–¥φ‘Ύ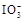 ΓΘΩ…Ι©―Γ”ΟΒΡΈο÷ ”–ΘΚΔΌΉ‘ά¥Υ°ΘΜΔΎάΕ…Ϊ ·»ο ‘÷ΫΘΜΔέΒβΜ·ΦΊΒμΖέ ‘÷ΫΘΜΔήΒμΖέΘΜΔί ≥¥ΉΘΜΔόΑΉΨΤΘΜΔΏ ≥Χ«ΓΘΡψ»œΈΣΫχ––…œ ω Β―ι ±±Ί–κ Ι”ΟΒΡΈο÷ «
Θ®Χν–ρΚ≈Θ©ΓΘ
ΓΘΩ…Ι©―Γ”ΟΒΡΈο÷ ”–ΘΚΔΌΉ‘ά¥Υ°ΘΜΔΎάΕ…Ϊ ·»ο ‘÷ΫΘΜΔέΒβΜ·ΦΊΒμΖέ ‘÷ΫΘΜΔήΒμΖέΘΜΔί ≥¥ΉΘΜΔόΑΉΨΤΘΜΔΏ ≥Χ«ΓΘΡψ»œΈΣΫχ––…œ ω Β―ι ±±Ί–κ Ι”ΟΒΡΈο÷ «
Θ®Χν–ρΚ≈Θ©ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com