
题目列表(包括答案和解析)
??
试以反应2Fe3++Fe![]() 3Fe2+设计一个原电池装置,并画出示意图,写出电极反应式。
3Fe2+设计一个原电池装置,并画出示意图,写出电极反应式。
??
试以反应2Fe3++Fe 3Fe2+设计一个原电池装置,并画出示意图,写出电极反应式.
3Fe2+设计一个原电池装置,并画出示意图,写出电极反应式.
A.正极发生氧化反应
B.负极反应式为Fe-3e-![]() Fe3+
Fe3+
C.能实现该反应的原电池是:正极为Cu,负极为Fe,电解质溶液为Fe2(SO4)3溶液
D.能实现该反应的原电池是:正极为Fe,负极为Zn,电解质溶液为FeCl3溶液
某原电池总反应为:2Fe3++Fe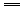 3Fe2+,不能实现该反应的原电池是
3Fe2+,不能实现该反应的原电池是
[ ]
A.正极为铜,负极为铁,电解质溶液为FeCl3
B.正极为银,负极为铁,电解质溶液为CuSO4
C.正极为铁,负极为锌,电解质溶液为Fe2(SO4)3
D.正极为碳,负极为铁,电解质溶液为Fe2(SO4)3
一、1.解析:Fe Fe2+
Fe2+ Fe3+
Fe3+ Fe(OH)3
Fe(OH)3 Fe2O3。
Fe2O3。
答案:A?
2.B 3.C?
4.解析:根据2Fe3++Fe===3Fe2+知,消耗1 mol Fe生成3 mol Fe2+,还消耗2 mol Fe3+。
答案:C?
5.C 6.A 7.B 8.A 9.C 10.AD?
二、11.Fe2O3 CO和H2 Fe3O4、FeO?
12.(1)白色沉淀 灰绿色
灰绿色 红褐色沉淀?
红褐色沉淀?
(2)3Fe+2NO +8H+===3Fe2++2NO↑+4H2O?
+8H+===3Fe2++2NO↑+4H2O?
(3)由反应2HNO3+NO===3NO2+H2O知,在浓HNO3中不可能生成NO?
13.(1)Fe Cl2 H2?
(2)2Fe+3Cl2 2FeCl3
2FeCl3
(3)2HCl+Fe===FeCl2+H2↑?
(4)2FeCl2+Cl2===2FeCl3?
14.(1)Fe FeCl3 FeCl2 Fe(OH)3 Fe2O3 (2)略?
15.65 g 20.5%?
16.(1)ac?
(2)设Fe2O3原有n0 mol,还原百分率为A%,则有?


A%= ≈33.3%
≈33.3%
(3)3-
(4)Fe2O3、Fe3O4 8<a<9?
Fe3O4、FeO 6<a<8?
Fe2O3、Fe3O4、FeO 6<a<9
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com