PCl
3可用于半导体生产的外延、扩散工序.有关物质的部分性质如下:
|
熔点/℃ |
沸点/℃ |
密度/g?mL |
其他 |
| 黄磷 |
44.1 |
280.5 |
1.82 |
2P(过量)+3Cl22PCl3
2P+5Cl2(过量)2PCl5 |
| PCl3 |
-112 |
75.5 |
1.574 |
遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 |
2 |
105.3 |
1.675 |
遇水生成H3PO4和HCl,能溶于
PCl3 |
(一)制备
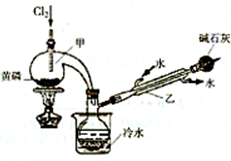
如图是实验室制备PCl
3的装置(部分仪器已省略)
(1)仪器乙的名称
冷凝管
冷凝管
;
(2)实验室制备Cl
2的离子方程式:
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
;
(3)碱石灰的作用是
吸收多余的氯气,防止污染环境
吸收多余的氯气,防止污染环境
,
防止空气中的水分进入影响产品
防止空气中的水分进入影响产品
;
(4)向仪器甲中通入干燥Cl
2之前,应先通入一段时间的CO
2,其目的是
排净装置中的空气,防止空气中的水分和氧气与PCl3反应
排净装置中的空气,防止空气中的水分和氧气与PCl3反应
.
(二)提纯
粗产品中常含有POCl
3、PCl
5等.加入黄磷加热除去PCl
5后,通过
蒸馏
蒸馏
(填实验操作名称),即可得到PCl
3的纯品.
(三)分析
测定产品中PCl
3纯度的方法如下:迅速称取m,g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c
1mol?L
-lV
1mL碘溶液,充分反应后再用c
2mol?L
-1Na
2S
2O
3溶液滴定过量的碘,终点时消耗V
2mLNa
2S
2O
3溶液.
已知:H
3PO
3+H
2O+I
2=H
3PO
4+2HI;I
2+2Na
2S
2O
3=2NaI+Na
2S
4O
6;假设测定过程中没有其他反应.根据上述数据,该产品中PCl
3的质量分数为
| (c1V1-c2V2)×137.5×20×10-3 |
| m |
×100%
| (c1V1-c2V2)×137.5×20×10-3 |
| m |
×100%
(用含字母的代数式表示、不必化简)

