
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
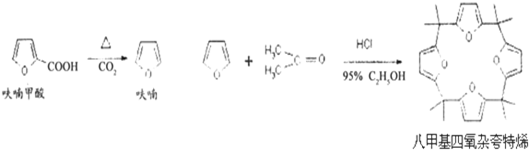
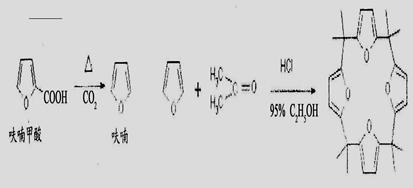
”…þª≤∏º◊À·Õ—Ù»µ√µΩþªý´”α˚Õ™‘⁄À·–‘Ãıº˛œ¬Àı∫œ£¨ø…µ√µΩ∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©°£”–πÿ µ—È‘≠¿Ìº∞¡˜≥ûÁœ¬£ª
≤Ω÷Ë1£∫þªý´µƒ÷∆±∏
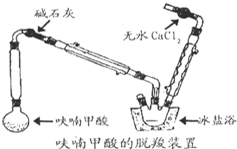
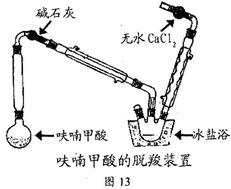
∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©‘⁄‘≤µ◊…’∆ø÷–∑≈÷√4.5gþªý´º◊À·£®100°Ê…˝ª™£¨þªý´º◊À·‘⁄133°Ê»€»⁄£¨230-232°Ê∑–Ã⁄£¨≤¢‘⁄¥ÀŒ¬∂»œ¬Õ—Ù»£©£¨∞¥Õº13∞≤◊∞∫√“«∆˜°£œ»¥Ûªº”»» πþªý´º◊À·øÏÀŸ»€ªØ£¨»ª∫Ûµ˜Ω⁄º”»»«ø∂»£¨≤¢±£≥÷Œ¢∑–£¨µ±þªý´º◊À·Õ—Ù»∑¥”¶Õͱœ£¨Õ£÷πº”»»°£µ√ŒÞ…´“∫ÃÂþªý´£®∑–µ„£∫31-32°Ê£¨“◊»Ð”⁄ÀÆ£©°£
≤Ω÷Ë2£∫¥Ûª∑ªØ∫œŒÔ∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©µƒ∫œ≥…‘⁄25mL◊∂–Œ∆ø÷–º”»Î2.7mL95%““¥º∫Õ1.35mL≈®—ŒÀ·£¨ªÏ‘»£¨‘⁄±˘‘°÷–¿‰÷¡5°Ê“‘œ¬£¨»ª∫ÛΩ´3.3mL±˚Õ™∫Õ1.35mLþªý´µƒªÏ∫œ“∫—∏ÀŸµπ»Î◊∂–Œ∆ø÷–£¨≥‰∑÷ªÏ‘»£¨±˘‘°¿‰»¥£¨æ≤÷√µ√“ªª∆…´¿Ø◊¥πÃð£π˝¬À£¨≤¢”√3mLŒÞÀÆ““¥ºœ¥µ”£Æ”√±Ω÷ÿΩ·æߣ¨µ√∞◊…´Ω·æß∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©°£
(1)≤Ω÷Ë1÷–”√¥Ûªº±ÀŸº”»»£¨∆‰÷˜“™ƒøµƒ « £ª
(2)◊∞÷√Õº÷–ºÓ ت“µƒ◊˜”√ « £ª
(3)Õ—Ù»◊∞÷√÷–”√±˘—Œ‘°µƒƒøµƒ « £ªŒÞÀƬ»ªØ∏∆µƒ◊˜”√ « £ª
(4)∫œ≥…∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©º”»Î—ŒÀ·µƒƒøµƒ « £ª
(5)»∑¬€≤˙∆∑Œ™∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©£¨ø…Õ®π˝≤‚∂®∑–µ„£¨ªπø…≤…”√µƒºÏ≤‚∑Ω∑®”– °£
”…þª≤∏º◊À·Õ—Ù»µ√µΩþªý´”α˚Õ™‘⁄À·–‘Ãıº˛œ¬Àı∫œ£¨ø…µ√µΩ∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©°£”–πÿ µ—È‘≠¿Ìº∞¡˜≥ûÁœ¬£ª
≤Ω÷Ë1£∫þªý´µƒ÷∆±∏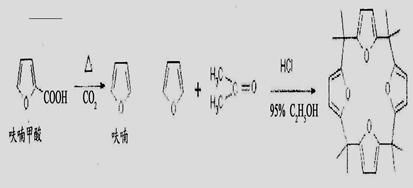
∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©‘⁄‘≤µ◊…’∆ø÷–∑≈÷√4.5gþªý´º◊À·£®100°Ê…˝ª™£¨þªý´º◊À·‘⁄133°Ê»€»⁄£¨230-232°Ê∑–Ã⁄£¨≤¢‘⁄¥ÀŒ¬∂»œ¬Õ—Ù»£©£¨∞¥Õº13∞≤◊∞∫√“«∆˜°£œ»¥Ûªº”»» πþªý´º◊À·øÏÀŸ»€ªØ£¨»ª∫Ûµ˜Ω⁄º”»»«ø∂»£¨≤¢±£≥÷Œ¢∑–£¨µ±þªý´º◊À·Õ—Ù»∑¥”¶Õͱœ£¨Õ£÷πº”»»°£µ√ŒÞ…´“∫ÃÂþªý´£®∑–µ„£∫31-32°Ê£¨“◊»Ð”⁄ÀÆ£©°£
≤Ω÷Ë2£∫¥Ûª∑ªØ∫œŒÔ∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©µƒ∫œ≥…‘⁄25mL◊∂–Œ∆ø÷–º”»Î2.7mL95%““¥º∫Õ1.35mL≈®—ŒÀ·£¨ªÏ‘»£¨‘⁄±˘‘°÷–¿‰÷¡5°Ê“‘œ¬£¨»ª∫ÛΩ´3.3mL±˚Õ™∫Õ1.35mLþªý´µƒªÏ∫œ“∫—∏ÀŸµπ»Î◊∂–Œ∆ø÷–£¨≥‰∑÷ªÏ‘»£¨±˘‘°¿‰»¥£¨æ≤÷√µ√“ªª∆…´¿Ø◊¥πÃð£π˝¬À£¨≤¢”√3mLŒÞÀÆ““¥ºœ¥µ”£Æ”√±Ω÷ÿΩ·æߣ¨µ√∞◊…´Ω·æß∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©°£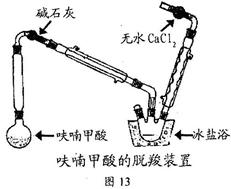
(1)≤Ω÷Ë1÷–”√¥Ûªº±ÀŸº”»»£¨∆‰÷˜“™ƒøµƒ « £ª
(2)◊∞÷√Õº÷–ºÓ ت“µƒ◊˜”√ « £ª
(3)Õ—Ù»◊∞÷√÷–”√±˘—Œ‘°µƒƒøµƒ « £ªŒÞÀƬ»ªØ∏∆µƒ◊˜”√ « £ª
(4)∫œ≥…∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©º”»Î—ŒÀ·µƒƒøµƒ « £ª
(5)»∑¬€≤˙∆∑Œ™∞Àº◊ª˘Àƒ—ı‘”ø‰Ãÿœ©£¨ø…Õ®π˝≤‚∂®∑–µ„£¨ªπø…≤…”√µƒºÏ≤‚∑Ω∑®”– °£

π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com