
题目列表(包括答案和解析)
| A、浓硫酸可用于干燥氢气、碘化氢等气体,但不能干燥氨气、二氧化氮气体 | B、将SO2通入溴水中,能使溴水褪色体现了SO2的还原性 | C、MgCl2、AlCl3溶液中分别加入过量的氨水来比较镁、铝的金属性强弱 | D、含FeCl3、CuCl2溶液中加入铁粉,充分反应后有固体剩余,加入KSCN溶液呈血红色 |
下列叙述正确的是?? ( )。
A.浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体,但不能干燥有较强还原性的HI、H2S等气体
B.浓硫酸与单质硫反应的化学方程式为:S+2H2SO4(浓)  3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
C.把足量铜粉投入到只含H2SO4 2 mol的浓硫酸中,得到气体体积标准状况下为22.4 L
D.常温下能够用铁、铝等容器盛放浓H2SO4,是因为浓H2SO4的强氧化性使其钝化
已知CN-、SCN-和Cl-有相似之处,两个—CN原子团和两个—SCN原子团可以分别组成氰分子(CN)2和硫氰分子(SCN)2,(CN)2和(SCN)2的性质与Cl2也有相似之处,常温常压下均为气体,它们的阴离子的还原性依次为:Cl-<Br-<CN-<SCN-<I-,它们都存在相应的氢化物HCN和HSCN。又已知浓H2SO4不能干燥HBr、HI。回答下列问题:
(1)在HCl、HBr、HCN、HSCN、HI中,能用浓H2SO4干燥的是____________________
________________________________。
(2)将(CN)2气体逐渐通入NaCl、NaBr、NaSCN和NaI的混合液中,发生反应的离子方程式是________________________________________。
(3)(CN)2和NaOH溶液反应的化学方程式是________________________________________
_________。其产物中的两种阴离子与SCN-相比,还原性顺序应是____________________
___________________________。
下列对浓硫酸的叙述正确的是
[ ]
A.浓硫酸具有吸水性,实验室中常用作气体干燥剂,但由于浓硫酸又具有强氧化性,因而它不能干燥具有还原性的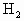 、CO等气体
、CO等气体
B.常温下,浓硫酸能使铁和铝表面钝化,所以铁质与铝质容器能盛放浓硫酸
C.浓硫酸和铜片加热反应,表现出强氧化性,又表现出酸性
D.浓硫酸与亚硫酸钠固体反应制取二氧化硫时,浓硫酸表现出强酸性
 3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com