
题目列表(包括答案和解析)
| 实验步骤 | 实验现象 | 解释和结论 |
| (1)在小烧杯中加入0.1mol/LFeCl3溶液2mL和0.1mol/LNH4SCN溶液2mL.加水10ml,混匀后分装于3支试管中. | 反应后形成红色溶液. | |
| (2) 往第一支试管加入少量三氯化铁溶液 往第一支试管加入少量三氯化铁溶液 |
试管中溶液 颜色加深 试管中溶液 颜色加深 |
增大反应物浓度促使 化学平衡向正反应的 方向移动 增大反应物浓度促使 化学平衡向正反应的 方向移动 |
| (3) 往第二支试管中加入少量硫氰化钾溶液 往第二支试管中加入少量硫氰化钾溶液 |
试管中溶液 颜色加深 试管中溶液 颜色加深 |
增大反应物浓度促使 化学平衡向正反应的 方向移动 增大反应物浓度促使 化学平衡向正反应的 方向移动 |
| (4)比较上述三支试管的颜色. | 加入铁离子或硫氰根离子都能使溶液 颜色加深 加入铁离子或硫氰根离子都能使溶液 颜色加深 |
增大任何一种反应物 的浓度促使化学平衡向正反应的方向移动 增大任何一种反应物 的浓度促使化学平衡向正反应的方向移动 |
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)图中A表示 ,E的大小对该反应的反应热有无影响? 。
(2)合成氨反应N2(g)+3H2(g)![]() 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂,反应的ΔH (填“增大”“减小”或“不改变”)。如果反应速率v(H2)为0.15 mol·L—1·min—1,则v(NH3)= mol·L—1·min—1
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂,反应的ΔH (填“增大”“减小”或“不改变”)。如果反应速率v(H2)为0.15 mol·L—1·min—1,则v(NH3)= mol·L—1·min—1
(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11, KsP[Cu(OH)2]=2.2×10-20。在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为 。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,当溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”)。
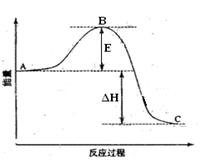
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)图中A表示 ,E的大小对该反应的反应热有无影响? 。
(2)合成氨反应N2(g)+3H2(g)2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂,反应的ΔH (填“增大”“减小”或“不改变”)。如果反应速率v(H2)为0.15mol·L—1·min—1,则v(NH3)= mol·L—1·min—1
(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11, KsP[Cu(OH)2]=2.2×10-20。在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为 。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,当溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”)。
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)图中A表示 ,E的大小对该反应的反应热有无影响? 。
(2)合成氨反应N2(g)+3H2(g)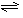 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂,反应的ΔH (填“增大”“减小”或“不改变”)。如果反应速率v(H2)为0.15
mol·L—1·min—1,则v(NH3)= mol·L—1·min—1
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂,反应的ΔH (填“增大”“减小”或“不改变”)。如果反应速率v(H2)为0.15
mol·L—1·min—1,则v(NH3)= mol·L—1·min—1
 (3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11, KsP[Cu(OH)2]=2.2×10-20。在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为 。
(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11, KsP[Cu(OH)2]=2.2×10-20。在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为 。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,当溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com