
题目列表(包括答案和解析)
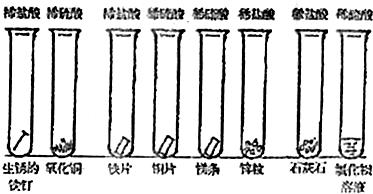
下列三组物质中,均有一种物质的类别与其它三种不同
A.MgO、Na2O、CO2、CuO
B.HCl、H2O、H2SO4、HNO3
C.NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A ;B C 。
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应 (“是”或“不是”)氧化还原反应。
(3)写出物质C与足量稀硫酸溶液反应的离子方程式: 。
(1)下列4组物质均有一种物质的类别与其它三种不同
A.CaO、Na2O、CO2、CuO B.H2、C、P、Cu
C.O2、Fe、Cu、Zn D.HCl、H2O、H2SO4、HNO3
以上四组物质中类别不同的物质依次是(填化学式)(各1分)
A ______;B __;C ;D 。
(2)写出下列物质在水溶液中的电离方程式:(各1分)
①氨水_________________________________________________________
②硫酸_________________________________________________________
③氢氧化钡_____________________________________________________
④硫酸铁_______________________________________________________
(3)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。(各2分)
A组: 。B组: 。
Ⅰ.某化学兴趣小组对下列三组物质进行研究:
A.HCl H2SO4 H2CO3 HNO3
B.溶液 水 悬浊液 胶体
C.Na2CO3 NaNO3 AgNO3 Ba(NO3)2
请你帮他们完善下列空白:
|
|
A |
B |
C |
|
分类标准 |
含氧酸 |
分散系 |
|
|
不属于该类别的物质 |
|
|
Na2CO3 |
Ⅱ.现有下列物质:①铝 ②氢氧化铁胶体 ③氯化氢 ④SO2 ⑤NaHSO4 固体 ⑥Ba(OH)2固体 ⑦稀硫酸 ⑧醋酸 ⑨烧碱 ⑩熔融NaNO3
(1)按物质的分类方法填写表格的空白处:(填编号)
|
分类标准 |
能导电的物质[ |
电解质 |
强电解质 |
|
属于该类的物质 |
|
|
|
(2)①与⑨的溶液反应的离子方程式为
(3)用Fe(OH)3胶体进行下列实验:
(a)将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附的颜色逐渐变 (填“深”或“浅”),这表明 。
(b)向其中逐滴加入过量稀硫酸溶液,现象是_______ _______;
(4)向Ba(OH)2溶液逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出此步的离子方程式 。
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看做是化学平衡的一种。请根据所学化学知识回答下列问题:
Ⅰ、(12分)已知0.01mol/L的NaHCO3溶液呈碱性。
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:
① ② 。
(2)溶液中共有 种不同的粒子(指分子和离子)。
(3)该溶液中的离子浓度由大到小的顺序是: 。
(4)向该溶液中加入AlCl3溶液,有白色胶状沉淀生成,同时产生一种无色无味并能使澄清石灰水变浑浊的气体,写出该反应的离子方程式: 。
Ⅱ、(6分)有盐酸、硫酸、醋酸三种溶液,试回答:
(1)若三种溶液的浓度均为0.1 mol•L-1,其c(H+) 依次为a mol•L-1,b mol•L-1,c mol•L-1,其大小顺序为 ;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小关系为 。
(2)若三种溶液的pH都为2,分别取10mL上述溶液加水稀释至1000mL,此时三种溶液的pH1、pH2、pH3之间的关系为 (用“<”、“>”或“=”表示,pH1 ——代表盐酸、 pH2 ——代表硫酸、pH3 ——代表醋酸)
Ⅲ、(4分)已知含有足量AgCl固体的饱和溶液中存在如下平衡:AgCl(s) Ag+(aq)+Cl-(aq),且在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl固体分别放入下列液体中:①100mL蒸馏水
Ag+(aq)+Cl-(aq),且在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl固体分别放入下列液体中:①100mL蒸馏水
②100mL0.3mol/L AgNO3溶液 ③100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)由大到小的顺序为 (填序号),溶液②中c(Cl-)= 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com