
题目列表(包括答案和解析)
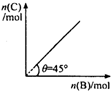 在盛有足量 A 的体积可变的密闭容器中,加入 B,发生反应:A(s)+2B(g)=4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时 C 的物质的量与加入的 B 的物质的量的变化关系如右图.下列说法正确的是( )
在盛有足量 A 的体积可变的密闭容器中,加入 B,发生反应:A(s)+2B(g)=4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时 C 的物质的量与加入的 B 的物质的量的变化关系如右图.下列说法正确的是( )| A、平衡时 B 的转化率为 50% | B、若再加入 B,则再次达到平衡时正、逆反应速率均增大 | C、若保持压强一定,再加人 B,则反应体系气体密度减小 | D、若保持压强一定,当温度升高 10℃后,则图中 θ>45° |
在盛有足量A的体积可变的密闭容器中,加入B,发生反应:A(s)+2B(g) 4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是

A.若保持压强一定,当温度升高后,则图中θ>45°
B.若再加入B,则再次达到平衡时正、逆反应速率均逐渐增大
C.若保持压强一定,再加入B,则反应体系气体密度减小
D.平衡时B的转化率为50%
在盛有足量A的体积可变的密闭容器中,加入B,发生反应:A(s)+2B(g)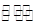 4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是( )
4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是( )
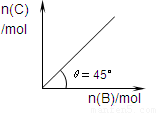
A.若保持压强一定,当温度升高后,则图中θ>45°
B.若再加入B,则再次达到平衡的过程中正、逆反应速率均逐渐增大
C.若保持压强一定,再加入B,则反应体系气体密度减小
D.平衡时B的转化率为50%
 4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是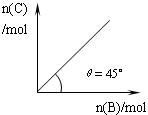
| A.若保持压强一定,当温度升高后,则图中θ>45° |
| B.若再加入B,则再次达到平衡时正、逆反应速率均逐渐增大 |
| C.若保持压强一定,再加入B,则反应体系气体密度减小 |
| D.平衡时B的转化率为50% |
 4C(g)+D(g) △H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如下图。下列说法正确的是
4C(g)+D(g) △H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如下图。下列说法正确的是 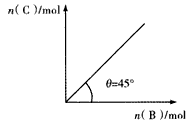
6B 7C 8D 9C 10B 11B 12A 13D
26 . ( 16 分)( 1 )第三(1 分)IA ( 1 分) ( 2 ) Na > N > H ( 2 分)
( 3 )正四面体结构(l 分)极性共价键(1 分)极性(1 分)
C2A2的电子式: ( 2 分)
( 2 分)

( 2 )防止碳酸钠液体倒吸,便于乙酸乙酯流出 ( 2 分)
( 3 ) I 98 %的浓硫酸具有强氧化性,使部分反应物炭化 ( 2 分)

II ① ② ③ (2 分,答一个且正确得1 分,有错不得分)10 mol?L一1 ( 2 分)
III 能(1 分)因为酯化反应的催化剂是H+,盐酸也能电离出H+ (2 分)
说明:1.本试卷中其它合理答案,可参照此评分标准酌情给分。
2.方程式未写条件或条件不完全、不写“↓”或“↑”均扣一分,不配平不得分。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com