
题目列表(包括答案和解析)
【解析】A项电荷守恒等式为:c(H+)+c(Na+)=c(OH-)+c(HSO3-)+c(HCO3-)+2c(CO32-) +2c(SO32-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(HSO3-)+c(HCO3-)+2c(CO32-)+2c(SO32-),A项不正确。
B项中的电荷守恒式为:c(Na+)+c(H+)=c(Cl-)+c(CH3COO-)+c(OH-),溶液呈中性,c(H+)=c(OH-),导出c(Na+)=c(Cl-)+c(CH3COO-);根据物料守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),由此二式导出c(Cl-)=c(CH3COOH),综上所述,有c(Na+)>c(Cl-)=c(CH3COOH),B项不对
C项中,NH4+水解呈酸性,CO32-水解呈碱性,它促进NH4+的水解;Fe2+水解呈酸性,它抑制NH4+的水解,所以三种溶液中c(NH4+):③>②>①,C项正确。
D项中,盐类的水解促进水的电离,强酸和弱酸都会抑制水的电离,当c(H+)相同时,对水的电离产生的抑制作用相同,正确的顺序应为①>②=③,D项不对。
【答案】C
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。下列说法中不正确的是:
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质:
【解析】若F是硫酸,则E是SO3,D是SO2,C是单质硫,则A可以是Na2S,B是硫化氢,A正确。当X是强碱时,A、B、C、D、E、F可以分别是NH4NO3、NH3、N2、NO、NO2、HNO3,B正确。氯气具有强氧化性,而C又是单质,所以反应一定氧化还原反应。所以选项D是错误的,答案选D。
向紫色Cr2(SO4)3溶液中,加入NaOH溶液至析出蓝灰色沉淀,此时,溶液中存在着如下平衡:Cr3+(紫色) +3OH- 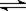 Cr(OH)3(蓝灰色)
Cr(OH)3(蓝灰色)  CrO2- (绿色)+H+ + H2O,将上述悬浊液等分两份a和b。向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液。a、b试管中溶液颜色最终分别为
CrO2- (绿色)+H+ + H2O,将上述悬浊液等分两份a和b。向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液。a、b试管中溶液颜色最终分别为
|
|
A |
B |
C |
D |
|
a试管 |
紫色 |
蓝灰色 |
蓝色 |
绿色 |
|
b试管 |
绿色 |
绿色 |
紫色 |
紫色 |
【解析】加入强碱会中和氢离子,平衡向正反应方向移动,溶液显绿色。加入强酸,会增大氢离子浓度,平衡向逆反应方向移动,溶液显紫色,所以答案是D。
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。下列说法中不正确的是:

A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质:
【解析】若F是硫酸,则E是SO3,D是SO2,C是单质硫,则A可以是Na2S,B是硫化氢,A正确。当X是强碱时,A、B、C、D、E、F可以分别是NH4NO3、NH3、N2、NO、NO2、HNO3,B正确。氯气具有强氧化性,而C又是单质,所以反应一定氧化还原反应。所以选项D是错误的,答案选D。
向紫色Cr2(SO4)3溶液中,加入NaOH溶液至析出蓝灰色沉淀,此时,溶液中存在着如下平衡:Cr3+(紫色) +3OH- Cr(OH)3(蓝灰色)
CrO2- (绿色)+H+ + H2O,将上述悬浊液等分两份a和b。向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液。a、b试管中溶液颜色最终分别为
|
| A | B | C | D |
| a试管 | 紫色 | 蓝灰色 | 蓝色 | 绿色 |
| b试管 | 绿色 | 绿色 | 紫色 | 紫色 |
【解析】加入强碱会中和氢离子,平衡向正反应方向移动,溶液显绿色。加入强酸,会增大氢离子浓度,平衡向逆反应方向移动,溶液显紫色,所以答案是D。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com