
题目列表(包括答案和解析)
(12分)两组同学对铁及其化合物的性质进行探究。
(1)一组同学用图1所示装置对铁与浓硫酸的反应进行实验。已知:
2Fe + 6H2SO4(浓) Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
①检查装置气密性后,将过量的铁屑和一定量的浓硫酸放入烧瓶,塞紧橡皮塞,开始计时t1时开始加热,在铁屑表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变。甲同学将收集到的气体体积与时间的关系粗略地表示为图2。
图1 图2
在0~t1时间段,铁屑表面没有气泡生成,说明铁在浓硫酸中发生了__________;t1~t2时间段,反应生成的气体是__________。
②t2时,取少量反应液,先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现红色褪去。同学们对红色褪去的原因提出各自的假设。乙同学的假设是:溶液中的+3价铁被氧化为更高的价态。你的另一种假设是__________;为了验证你的假设,请设计一种简便的实验方案__________。
(2)另一组同学对铁和稀硝酸的反应进行探究。他们用a mol Fe和含有b mol HNO3的稀硝酸进行实验,若HNO3只被还原成NO,且反应结束后溶液中含有Fe3+和Fe2+,则a/b的取值范围是__________;若反应结束后的溶液中n(Fe3+):n(Fe2+)=2:1,则的值为__________。
A.Fe2+ B.Mg2+ C.Cl- D.Ba2+
A.3∶4 B.3∶5 C.4∶3 D.3∶2
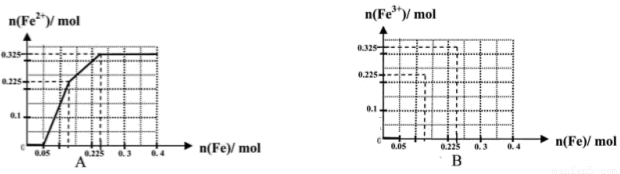
(一)(8分)在含有物质的量各为0.1 mol FeCl3、H2SO4、Cu(NO3)2的溶液500 mL中,逐渐加入铁粉,溶液中n(Fe2+)与加入n(Fe)的关系如图A(请注意识图,该题图中每小正方格长度为0.05mol)。(提示:忽略离子水解产生的影响;如果有硝酸根被还原时,则生成一氧化氮气体)
(1)写出图中n(Fe)从0.125mol-0.225 mol段对应反应的离子方程式____。
(2)写出图中n(Fe)从0-0.05 mol段对应反应的离子方程式____。
(3)请在图B中画出溶液中n(Fe3+)与加入n(Fe)的变化关系图
(4)当反应进行到最后,取该溶液2mL加入试管中,为了证明该溶液中有NO3-存在,可以向试管中在滴加_______。
A.酸性KMnO4溶液??? B.含有盐酸的KSCN溶液??? C.碘水??? D.次氯酸钠溶液
(二)(5分)下图是电解槽的剖面图,箭头的方向指的是气体或溶液的流向,阳离子交换膜只允许阳离子通过。现要用此装置来通过电解分离Na2SO4和NaOH的混合溶液,则向装置中通入A1溶液和A2溶液(A1溶液是Na2SO4和NaOH的混合溶液,A2溶液是NaOH的稀溶液)。电解一段时间后,装置中流出:B2溶液(是NaOH的浓溶液)和B1溶液,C1气体和C2气体。
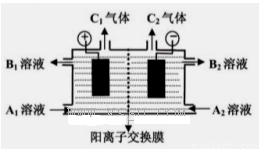
(1) C2气体是______(填化学式)。
(2)请写出阳极反应的电极方程式???????????????????????????????? .
(3)请简述阴极室能流出NaOH的浓溶液的原因????????????????????????? .
含有1mol HNO3的稀硝酸分别与不同质量的铁粉反 应, 所得氧化产物a、b与铁粉物质的量关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断正确的是
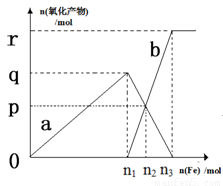
A.a是Fe(NO3)3 B.n1 = 0.375
C.p点时,n(Fe3+)=0.15mol D.n2 = 0.50
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com