
题目列表(包括答案和解析)
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。

①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1=15 s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________
向某密闭容器中加人0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[t0~tl阶段的c(B)变化未画出]。乙图为t2时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同,t3~t4阶段为使用催化剂。下列说法中不正确的是

A.若tl=15s,则用C的浓度变化表示的t0~tl段的平均反应速率为0.004mol?L-1?s-1
B.以t4~t5阶段改变的条件一定为减小压强
C.该容器的容积为2 L, B的起始物质的量为0.02mo1.
D.t5~t6阶段,容器内A的物质的量减少了0.03mol,而此过程中容器与外界的热交换总量为akJ,该反应的热化学方程式为:3A(g)![]() B(g) + 2C(g);△H =+100a kJ?mo1-1
B(g) + 2C(g);△H =+100a kJ?mo1-1
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:?NaIO3+?NaHSO3→?I2+?Na2SO4+?H2SO4+?H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1="15" s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用 催化剂 b增大压强 c增大反应物浓度
催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1=15 s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________
研究化学反应原理对于生产生活是很有意义的。
(1)下列关于醋酸的叙述正确的是 (填写符号)。
a.等体积等pH的醋酸和盐酸完全被NaOH溶液中和,消耗NaOH的物质的量一样多
b.向醋酸溶液中加入一定量NaOH固体,溶液的导电性增强
c.加水稀释醋酸溶液,溶液中的所有离子浓度均减小
d.常温下,醋酸溶液中水的电离程度比纯水的小
(2)钢铁生锈现象随处可见,钢铁的电化腐蚀原理如图所示:
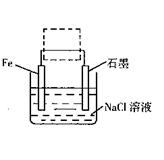
①写出石墨电极的电极反应式 ;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改。
③写出修改后石墨电极的电极反应式 。
(3)①高炉炼铁过程中会发生反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g)。
Fe(s)+CO2(g)。
已知:Fe(s)+1/2O2(g)=FeO(s)△H= -272kJ·mol-1
C(s)+O2(g)=CO2(g) △H= -393.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H= -22lkJ·mol-1
则:①FeO(s)+CO(g)![]() Fe(s)+CO2(g)
Fe(s)+CO2(g)
△H= 。
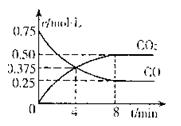
②一定温度下,向某密闭容器中加人足量FeO,
并充人一定量的CO气体,反应过程中CO和CO2的
浓度与时间的关系如图所示则从开始至达到平衡过程中,![]() (CO)= 。
(CO)= 。
(4)铁红是一种红色颜料,其成份是Fe2O3。将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加人一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com