
题目列表(包括答案和解析)
某氧化还原反应的离子方程式的已知部分为:2口+5口+口H+=5口+2口十8口
试根据该反应式和下表提供的材料回答下列问题和第8题
序号 | 氧化剂 | 还原剂 | 其它反应物 | 氧化产物 | 还原产物 |
(1) | Cl2 | FeBr2 | / | FeCl3 | |
(2) | KMnO4 | H2O2 | H2SO4 | O2 | MnSO4 |
(3) | KClO3 | HCl(浓) | / | Cl2 | Cl2 |
(4) | KMnO4 | HCl(浓) | / | Cl2 | MnCl2 |
若对应于上述离子方程式的电子转移总数为10,则反应物、生成物的组序号是( )。
A、(2)、(4) B.只有(2)
C、只有(4) D.只有(3)
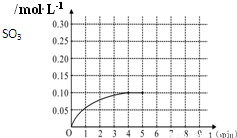
 一定温度下,将0.4molSO2和0.2molO2放入固定容积为2L的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol,反应中SO3的物质的量浓度的变化情况如图:
一定温度下,将0.4molSO2和0.2molO2放入固定容积为2L的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol,反应中SO3的物质的量浓度的变化情况如图:(07年江苏卷) (8分)在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050mol?L-1(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式。
(2)试通过计算确定该钠块中钠元素的质量分数。
(05年上海卷)在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:
H2(g)+I2(g)![]() 2HI(g)+Q(Q>0)
2HI(g)+Q(Q>0)
反应中各物质的浓度随时间变化情况如图1:
(1)该反应的化学平衡常数表达式为 ;
(2)根据图1数据,反应开始至达到平衡时,平均速率v(HI)为 ;
(3)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K(填写增大、减小或不变)HI浓度的变化正确 ;
(用图2中a~c的编号回答)
②若加入I2,H2浓度的变化正确的是 。(用图2中d~f的编号回答)
(4)反应达到平衡后,第8分钟时,若反容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况。



湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com