
题目列表(包括答案和解析)
| ||
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铜绿的主成分是碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
| B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 铁比铜活泼 | 例在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
| D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
(10分) CO2和NaOH的反应是一个很基本的化学反应,有很多的实验方法可以通过观察到的明显现象说明CO2与NaOH溶液发生了反应.现提供如下实验用品:集气瓶、烧瓶、分液漏斗、长颈漏斗、导管、橡皮管、弹簧夹、烧杯、量筒、水、CO2气体、NaOH溶液以及你认为所能用到的仪器和药品.现有五位同学设计了如图所示的A~E五个装置,试回答:
(1)对图A,当将分液漏斗中的NaOH溶液滴入烧瓶时,如果看到水槽中的水被吸入到烧瓶中,则证明CO2与NaOH溶液发生了反应.请写出此过程中NaOH溶液与CO2可能发生的反应离子方程式:__________________、____________________.
(2)对图B~E,请指出能达到实验目的的装置______________(用B、C、D、E填空).B中出现_______________________现象可证明CO2与NaOH发生了反应.
(3)将标准状况下一定体积的CO2气体缓慢通入V L NaOH溶液中,结果CO2和NaOH均无剩余.在反应后的溶液中加入足量的澄清石灰水得到W g沉淀.据以上数据能否确定CO2的体积?若能,请用上述数据求出CO2的体积.若不能,还需做什么实验?简要说明并运用实验测得的数据列式表示._________________________________________
(1)B固体中所包含的化学键有____________、____________。(填化学键的类型)
(2)反应①的化学方程式为____________________________________,反应⑤的离子方程式为_________________________________________________________________。
(3)工业上反应③的条件是_______________________________________________。
(4)在工业上G是如何转化为H的?___________________________________________。
(10分) CO2和NaOH的反应是一个很基本的化学反应,有很多的实验方法可以通过观察到的明显现象说明CO2与NaOH溶液发生了反应.现提供如下实验用品:集气瓶、烧瓶、分液漏斗、长颈漏斗、导管、橡皮管、弹簧夹、烧杯、量筒、水、CO2气体、NaOH溶液以及你认为所能用到的仪器和药品.现有五位同学设计了如图所示的A~E五个装置,试回答:
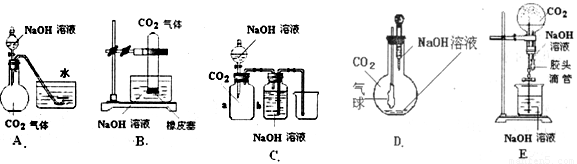
(1)对图A,当将分液漏斗中的NaOH溶液滴入烧瓶时,如果看到水槽中的水被吸入到烧瓶中,则证明CO2与NaOH溶液发生了反应.请写出此过程中NaOH溶液与CO2可能发生的反应离子方程式:__________________、____________________.
(2)对图B~E,请指出能达到实验目的的装置______________(用B、C、D、E填空).B中出现_______________________现象可证明CO2与NaOH发生了反应.
(3)将标准状况下一定体积的CO2气体缓慢通入V L NaOH溶液中,结果CO2和NaOH均无剩余.在反应后的溶液中加入足量的澄清石灰水得到W g沉淀.据以上数据能否确定CO2的体积?若能,请用上述数据求出CO2的体积.若不能,还需做什么实验?简要说明并运用实验测得的数据列式表示._________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com