
题目列表(包括答案和解析)

| ||
| ||
| ||
| ||
实验室获取氮气有很多种途径,常见的3种方法是:
方法一:将氨气通人灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
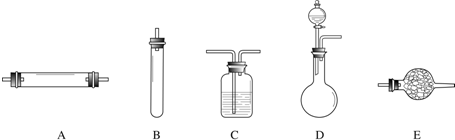
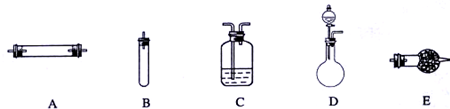
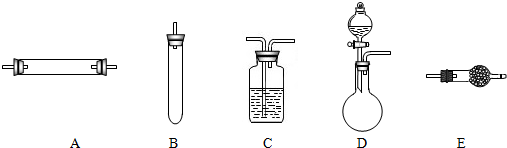
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气,产物中还含有相对分子量最小的氧化物。进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
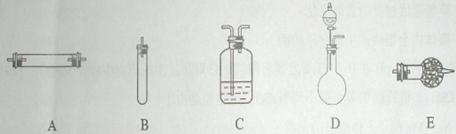
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用 (选填装置编号)。请写出生石灰在此反应中的作用:__________________________________
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置_ ________(选填装置编号)中加入 以除去其它杂质气体。
(3)方法三:制氮气的化学方程式为 。
(4)1892年,英国科学家瑞利(( Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大50‰。左右。若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:_______________ _________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com