
题目列表(包括答案和解析)
31.(6分)小婧同学做硫在氧气中燃烧的实验前,预先在集气瓶底装有少量水。实验过程中她联想到老师介绍过二氧化硫排放到空气中会形成酸雨,于是想了解燃烧后集气瓶底部残留的“水”是否也呈酸性。她取“水”多次测其pH,发现其pH始终小于7并逐渐减小,直至稳定在pH=4,证明集气瓶底残留液呈 性。随后小婧想进一步了解该残留液是否具有酸的通性,请你与她一起探究:
[提出问题]残留液还能与什么物质反应呢?
[猜想]① ;② ;
[设计方案]请你设计实验来验证你的猜想:(选择一个猜想即可)
| 实验方法 | 可能观察到的现象 | 结论 |
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
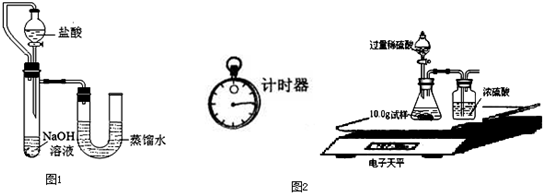
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
| 物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com