
题目列表(包括答案和解析)
(每空2分,共16分)短周期元素X、Y、Z、W,原子序数依次增大。常温常压下,只有W的单质为气体。它们的最高氧化物对应的水化物依次为甲、乙、丙、丁。甲、乙、丙是中学化学中的常见物质,其中只有乙难溶于水,且能和甲、丙反应得到澄清溶液。根据以上信息填写下列空白:
⑴画出W的原子结构示意图_________________________________________;
⑵将乙和甲、丙分别反应后得到的溶液混合,观察到的现象是___________________
___________________ ,两溶液混合时所发生反应的离子方程式为____________________________________________________;
⑶下列事实能证明Z和W非金属性强弱的是(选填序号)__________________________;
| A.单质的熔点:Z>W2 |
| B.酸性:丁>丙 |
| C.在溶液中:W2+H2Z=2HW+Z |
| D.稳定性:HW>H2Z |
(每空2分,共16分)短周期元素X、Y、Z、W,原子序数依次增大。常温常压下,只有W的单质为气体。它们的最高氧化物对应的水化物依次为甲、乙、丙、丁。甲、乙、丙是中学化学中的常见物质,其中只有乙难溶于水,且能和甲、丙反应得到澄清溶液。根据以上信息填写下列空白:
⑴画出W的原子结构示意图_________________________________________;
⑵将乙和甲、丙分别反应后得到的溶液混合,观察到的现象是___________________
___________________ ,两溶液混合时所发生反应的离子方程式为____________________________________________________;
⑶下列事实能证明Z和W非金属性强弱的是(选填序号)__________________________;
A.单质的熔点:Z>W2 B.酸性:丁>丙
C.在溶液中:W2+H2Z=2HW+Z
D.稳定性:HW>H2Z E.氢化物水溶液的酸性:HW>H2Z
F.溶解性:丁>丙
⑷用Y单质和生活中最常用的金属作电极,用导线连接插入甲的溶液中构成原电池,该原电池负极的电极反应式为_______________________________________________ ;
⑸工业上以XW为原料可以进行许多化生产,甲和W2都是其主要产品。写出工业上以XW为原料生产甲和W2的化学方程式_______________________________________________
_______________________________________________;若要生产80.0 kg甲物质,至少需要XW______________kg,同时可得W2_____________m3(标况)。
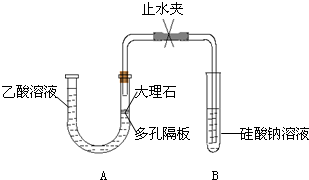
Ⅰ.探究乙酸、碳酸和硅酸的酸性强弱关系,该小组设计了如下实验装置(夹持仪器已略去)。

(1)实验前如何检查装置A的气密性?______________________________。
(2)装置A中反应产生的气体通入试管B溶液中,有白色胶状沉淀生成,说明碳酸酸性比硅酸强。
有学生认为B中的实验现象不足以证明碳酸的酸性比硅酸强,理由是:
a.乙酸易挥发,乙酸气体随CO2气体进入试管B的溶液中,和硅酸钠溶液反应生成沉淀。
b.该复分解反应生成的硅酸是难溶固体,不能说明是因为生成弱酸而发生反应。
为了证明碳酸能和硅酸钠反应生成硅酸沉淀,下列方法中可行的是__________(填序号)。
①在仪器A、B之间连接盛有足量饱和NaHCO3溶液的洗气瓶
②在仪器A、B之间连接装有足量碱石灰的干燥管
③在仪器A、B之间连接盛有足量饱和Na2CO3溶液的洗气瓶
④用碳酸钠粉末代替大理石进行实验
下列能够说明碳酸比硅酸酸性强的事实是__________(填序号)。
①相同温度时,碳酸的溶解度比硅酸的溶解度大
②碳酸比硅酸易分解
③相同温度下,相同物质的量浓度的Na2CO3和Na2SiO3溶液,Na2CO3溶液的pH比Na2SiO3溶液的pH小
④常温下,CO2是气体,SiO2是固体
Ⅱ.证明乙酸为弱酸。
现有常温下pH=3的乙酸溶液、蒸馏水、石蕊试液及pH试纸,用最简便的实验方法证明乙酸为弱酸:________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com