
题目列表(包括答案和解析)
分析下列氧化还原反应中化合价的变化,指出氧化剂和还原剂.
(1)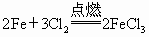 ,氧化剂为__________,还原剂为___________.
,氧化剂为__________,还原剂为___________.
(2) ,氧化剂为_________,还原剂为
,氧化剂为_________,还原剂为
___________.
(3)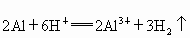 ,氧化剂为________,还原剂为_________.
,氧化剂为________,还原剂为_________.
(4)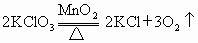 ,氧化剂为___________,__________.
,氧化剂为___________,__________.
分析下列氧化还原反应中化合价的变化,指出氧化剂和还原剂.
(1)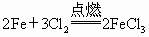 ,氧化剂为__________,还原剂为___________.
,氧化剂为__________,还原剂为___________.
(2) ,氧化剂为_________,还原剂为
,氧化剂为_________,还原剂为
___________.
(3) ,氧化剂为________,还原剂为_________.
,氧化剂为________,还原剂为_________.
(4) ,氧化剂为___________,__________.
,氧化剂为___________,__________.
(1)2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(2)2Fe2O3+3C![]() 4Fe+3CO2
4Fe+3CO2
(3)3NO2+H2O![]() 2HNO3+NO
2HNO3+NO
(4)HgS+O2![]() Hg+SO2
Hg+SO2
(5)2H2S+SO2![]() 3S+2H2O
3S+2H2O
分析下列氧化还原反应中化合价的变化关系,注明电子转移方向和总数,并指出氧化剂和还原剂,氧化产物与还原产物,属于四种基本反应类型的具体指出其反应类型.
(1)2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(2)2Fe2O3+3C![]() 4Fe+3CO2
4Fe+3CO2
(3)3NO2+H2O![]() 2HNO3+NO
2HNO3+NO
(4)HgS+O2![]() Hg+SO2
Hg+SO2
(5)2H2S+SO2![]() 3S+2H2O
3S+2H2O
分析下列氧化还原反应中化合价的变化关系,注明电子转移方向和总数,并指出氧化剂和还原剂,氧化产物与还原产物,属于四种基本反应类型的具体指出其反应类型.
(1)2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(2)2Fe2O3+3C![]() 4Fe+3CO2
4Fe+3CO2
(3)3NO2+H2O![]() 2HNO3+NO
2HNO3+NO
(4)HgS+O2![]() Hg+SO2
Hg+SO2
(5)2H2S+SO2![]() 3S+2H2O
3S+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com