
题目列表(包括答案和解析)
短周期元素A、B、C、D、E、F的原子序数依次增大,其元素特征信息如下表:
| 元素编号 | 元素特征信息 |
| A | 阳离子核外无电子 |
| B | 最高正价和最低负价的绝对值之差为2 |
| C | 最外层电子数是内层电子数的3倍 |
| D | 1molC单质能与冷水反应,在标准状况下生成11.2LH2 |
| E | 原子最外层电子数等于其周期序数 |
| F | 负二价阴离子的电子层结构与Ar原子相同 |
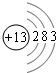
(1)F的简单离子的结构示意图为____________;
(2) E在周期表中的位置为 ________________;
(3)C和D简单离子的半径大小为__________;(用离子符号和“>”、“=”或“<”表示)
(4)元素非金属性强弱比较有很多方法,其中C和F的非金属性强弱的研究方案中不可行的是_________(填序号);
a.比较两种单质的颜色 b.比较氢化物的稳定性
c.依据两元素在周期表中的位置 d.依据两元素单质在自然界中的存在状态
(5) A、C、D三种元素组成的化合物中含有的化学键为________ ;
写出E的单质与上述化合物的水溶液反应的离子方程式:
__________________________________________________________________。

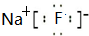
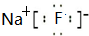
18 8 |
18 8 |

X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的常见化合价为+3。回答下列问题:
(1)Y-的结构示意图为 。
(2)写出含有10个中子的X原子的原子符号 。
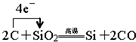
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目 。
(4)向WY3溶液中加入足量的NaOH溶液,反应的离子方程式为 。
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为 。
(6)ZX2中存在的化学键为 (填“离子键”或“共价键”),ZX2与NaOH溶液反应的化学方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com