
题目列表(包括答案和解析)
 下图是元素R的单质及其重要化合物在一定条件下相互转化的关系图(生成物中不含该元素的物质均已略去).已知F可用作化肥,也可用来制炸药;G可用于作防腐剂或建筑工程上的抗冻剂.据此回答以下问题:
下图是元素R的单质及其重要化合物在一定条件下相互转化的关系图(生成物中不含该元素的物质均已略去).已知F可用作化肥,也可用来制炸药;G可用于作防腐剂或建筑工程上的抗冻剂.据此回答以下问题: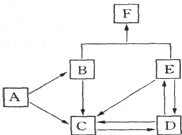 如图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去).其中A是单质,D在常温下呈气态,F可用作氮肥.
如图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去).其中A是单质,D在常温下呈气态,F可用作氮肥.
| ||
| △ |
| ||
| △ |

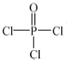 )与季戊四醇(
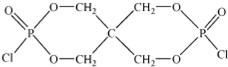
)与季戊四醇(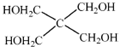 )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体.季戊四醇与X 的核磁共振氢谱如图所示.
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体.季戊四醇与X 的核磁共振氢谱如图所示.

(10分)下图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去)。其中A是单质,D在常温下呈气态,F可用作氮肥。
据此,请回答下列问题:
(1)写出物质的化学式:A ,D ,F 。
(2)写出下列变化的化学方程式:
B→C 。
E→C 。
(1)钛元素的同位素有:![]() 、
、![]() 、
、![]() 、
、![]() ,则下列说法正确的是( )
,则下列说法正确的是( )
A.可计算出钛元素的相对原子质量为48
B.钛元素的五种同位素化学性质均不相同
C.钛元素在元素周期表中位于第四周期
D.钛与铁(26Fe)同为第Ⅷ族元素
(2)TiO2(二氧化钛)是高级的白色颜料,它可用下列反应制得:
第一步:FeTiO3+2H2SO4====TiOSO4+FeSO4+2H2O,此时钛铁矿中的Fe2O3也与H2SO4发生反应,可加入铁屑使其还原成Fe2+,写出此过程的离子反应方程式:____________________。
第二步:TiOSO4+2H2O![]() TiO2·H2O+H2SO4-Q,制二氧化钛的关键是第二步水解反应。为使第二步反应进行得更完全,可采用下列_______措施。
TiO2·H2O+H2SO4-Q,制二氧化钛的关键是第二步水解反应。为使第二步反应进行得更完全,可采用下列_______措施。
A.加酸 B.加碱 C.加热 D.加压
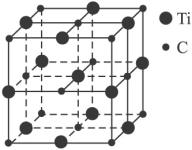
(3)最近发现一种由钛原子和碳原子构成的气态团簇分子,如图所示,则它的化学式为_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com