
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈ1ЃЉaЕчМЋВФСЯгІЮЊ________ЃЌЕчМЋЗДгІЪНЮЊ________ЁЃ
ЃЈ2ЃЉЕчНтвКcПЩвдЪЧЃЈЬюБрКХЃЉ________ЁЃ
AЃЎДПЫЎЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎNaClШмвК
CЃЎNaOHШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎCuCl2ШмвК
ЃЈ3ЃЉdЮЊБНЃЌЦфзїгУЮЊ________ЃЌдкМгШыБНжЎЧАЃЌЖдcгІзїКЮМђЕЅДІРэЃП________ЁЃ
ЃЈ4ЃЉЮЊСЫдкНЯЖЬЪБМфФкПДЕНАзЩЋГСЕэЃЌПЩВЩШЁЕФДыЪЉЪЧЃЈЬюБрКХЃЉ________ЁЃ
AЃЎИФгУЯЁСђЫсзїЕчНтвКЁЁЁЁЁЁЁЁ BЃЎЪЪЕБдіДѓЕчдДЕФЕчбЙ
CЃЎЪЪЕБМѕЩйСНЕчМЋМфОрРыЁЁЁЁ DЃЎЪЪЕБНЕЕЭЕчНтвКЕФЮТЖШ
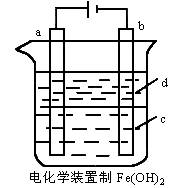
гЩгкFe(OH)2МЋвзБЛбѕЛЏЃЌЫљвдЪЕбщЪвКмФбгУбЧЬњбЮШмвКгыЩеМюЗДгІжЦЕУАзЩЋДПОЛFe(OH)2ГСЕэЁЃгІгУШчЭМЕчНтЪЕбщПЩжЦЕУАзЩЋЕФДПОЛFe(OH)2ГСЕэЁЃСНЕчМЋЕФВФСЯЗжБ№ЮЊЪЏФЋКЭЬњЁЃ
ЃЈ1ЃЉaЕчМЋВФСЯгІЮЊ________ЃЌЕчМЋЗДгІЪНЮЊ________ЁЃ
ЃЈ2ЃЉЕчНтвКcПЩвдЪЧЃЈЬюБрКХЃЉ________ЁЃ
AЃЎДПЫЎЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎNaClШмвК
CЃЎNaOHШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎCuCl2ШмвК
ЃЈ3ЃЉdЮЊБНЃЌЦфзїгУЮЊ________ЃЌдкМгШыБНжЎЧАЃЌЖдcгІзїКЮМђЕЅДІРэЃП________ЁЃ
ЃЈ4ЃЉЮЊСЫдкНЯЖЬЪБМфФкПДЕНАзЩЋГСЕэЃЌПЩВЩШЁЕФДыЪЉЪЧЃЈЬюБрКХЃЉ________ЁЃ
AЃЎИФгУЯЁСђЫсзїЕчНтвКЁЁЁЁЁЁЁЁ BЃЎЪЪЕБдіДѓЕчдДЕФЕчбЙ
CЃЎЪЪЕБМѕЩйСНЕчМЋМфОрРыЁЁЁЁ DЃЎЪЪЕБНЕЕЭЕчНтвКЕФЮТЖШ

ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com