
题目列表(包括答案和解析)
为探索乙醇氧化的反应机理,某研究性学习小组的学生设计了下列实验方案。
(1) 将一根粗铜丝绕成螺旋状,称量得到数值m1 g ;
(2) 取一支试管,加入3 mL 乙醇;
(3) 把上述已称量过的铜丝放在酒精灯火焰上加热至红热后稍冷,可看到铜丝___________
_______________________________(填写现象),称量得到数值 m2 g,并且m2_____ m1 (填“大于”、“小于”或“等于”)
(4) 将冷却后的铜丝伸入试管里的酒精溶液中,可看到铜丝________________________(填写现象)
(5) 若将红热的铜丝伸入试管里的酒精溶液中,可看到铜丝________________________(填写现象)
(6) 反复多次后,可闻到试管里溶液有____________________________________________;
(7) 最后将从酒精溶液中取出的铜丝烘干后称量,得到数值 m3 ,则m3_____________ m1(填“大于”、“小于”或“等于”)
(8) 步骤(3)中的化学反应方程式为_____________________________,步骤(5)中的化学方程式为_____________________,总的反应方程式为___________________________。
教材中给出了Na2O2与H2O反应的化学方程式。为了探究Na2O2与H2O反应的机理,某学习探究小组在教师指导下设计了如下图所示装置进行实验。

实验步骤如下:
①按图示组装仪器,并检查气密性为良好后装入药品;
②保持K1打开、K2关闭,将注射器中的水推入试管,此时A中无气体产生;
③挤压装有酚酞的胶头滴管,使酚酞滴入试管中,A中溶液显红色;
④挤压装有稀盐酸的胶头滴管,使稀盐酸滴入试管中,红色消失后再滴加2滴;
⑤用双连打气球向A中鼓气,使A中溶液通过喷头进入B中支管,发现淀粉KI溶液变蓝,KMnO4溶液褪色;
⑥迅速打开止水夹K2,关闭K1,继续向A中鼓气,待A中溶液进入C中约三分之一时停止鼓气。然后用热水浴加热C片刻,C中有气泡冒出,经检验为氧气。
回答下列问题:
(1) 写出Na2O2与H2O反应的离子方程式 ;
(2)若向Na2O2中滴加适量的盐酸,也能产生使带火星的木条复燃的气体,且最后溶液呈中性,请写出该反应的化学方程式 ;
(3)用离子方程式表示淀粉KI溶液变蓝的原因_____________________________ _;
(4)用离子方程式表示KMnO4溶液褪色的原因(MnO4-在酸性条件下被还原成Mn2+)
____________________________ ___ ;
(5)A中用冰盐冷浴和C中用热水浴的作用分别是________________________ ____,
;
(6)Na2O2与H2O反应的机理是(用化学方程式表示)______________________ ___,
。
(13分)某学习小组甲利用中和反应原理和DIS系统(即数字化信息系统,由传感器、数据采集器和计算机组成)测定某氨水的物质的量浓度,以测量溶液导电能力来判断滴定终点。请回答:
(1)实验时量取10.00mL氨水样品,配制成100mL待测氨水,则该步操作中需要的仪器有_________________(填仪器名称)。
(2)量取20.00mL上述溶液倒入洁净干燥锥形瓶中,连接好DIS系统。如果锥形瓶中含有少量蒸馏水,是否会影响测量结果_______(填“是”“否”“不能确定”)。
(3)①滴定管盛放盐酸前,要先__________________,用少量蒸馏水洗涤后,再_________________,然后加入盐酸调整液面至凹液面的最低点处于滴定管的_________________。
②向锥形瓶中滴加0.10mol·L-1的盐酸,计算机屏幕上显示出溶液导电能力与加入盐酸体积关系的曲线图。
写出氨水与盐酸反应的离子方程式___________________________;该氨水样品的物质的量浓度为_____________。
(4)另一学习小组乙认为上述测量结果仍存在一定误差,因为生成的NH4Cl 是强酸弱碱盐,会发生水解而使NH4+ 浓度下降,这样,恰好完全反应时NH4+ 浓度不是最大值,溶液导电性就不是最大值。你认为乙学习小组的结论是否正确?________,理由是___________________。
(13分)某学习小组甲利用中和反应原理和DIS系统(即数字化信息系统,由传感器、数据采集器和计算机组成)测定某氨水的物质的量浓度,以测量溶液导电能力来判断滴定终点。请回答:
(1)实验时量取10.00mL氨水样品,配制成100mL待测氨水,则该步操作中需要的仪器有_________________(填仪器名称)。
(2)量取20.00mL上述溶液倒入洁净干燥锥形瓶中,连接好DIS系统。如果锥形瓶中含有少量蒸馏水,是否会影响测量结果_______(填“是”“否”“不能确定”)。
(3)①滴定管盛放盐酸前,要先__________________,用少量蒸馏水洗涤后,再_________________,然后加入盐酸调整液面至凹液面的最低点处于滴定管的_________________。
②向锥形瓶中滴加0.10mol·L-1的盐酸,计算机屏幕上显示出溶液导电能力与加入盐酸体积关系的曲线图。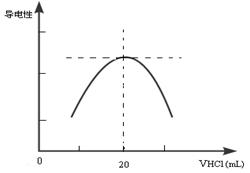
写出氨水与盐酸反应的离子方程式___________________________;该氨水样品的物质的量浓度为_____________。
(4)另一学习小组乙认为上述测量结果仍存在一定误差,因为生成的NH4Cl 是强酸弱碱盐,会发生水解而使NH4+浓度下降,这样,恰好完全反应时NH4+浓度不是最大值,溶液导电性就不是最大值。你认为乙学习小组的结论是否正确?________,理由是___________________。
(13分)某学习小组甲利用中和反应原理和DIS系统(即数字化信息系统,由传感器、数据采集器和计算机组成)测定某氨水的物质的量浓度,以测量溶液导电能力来判断滴定终点。请回答:
(1)实验时量取10.00mL氨水样品,配制成100mL待测氨水,则该步操作中需要的仪器有_________________(填仪器名称)。
(2)量取20.00mL上述溶液倒入洁净干燥锥形瓶中,连接好DIS系统。如果锥形瓶中含有少量蒸馏水,是否会影响测量结果_______(填“是”“否”“不能确定”)。
(3)①滴定管盛放盐酸前,要先__________________,用少量蒸馏水洗涤后,再_________________,然后加入盐酸调整液面至凹液面的最低点处于滴定管的_________________。
②向锥形瓶中滴加0.10mol·L-1的盐酸,计算机屏幕上显示出溶液导电能力与加入盐酸体积关系的曲线图。

写出氨水与盐酸反应的离子方程式___________________________;该氨水样品的物质的量浓度为_____________。
(4)另一学习小组乙认为上述测量结果仍存在一定误差,因为生成的NH4Cl 是强酸弱碱盐,会发生水解而使NH4+ 浓度下降,这样,恰好完全反应时NH4+ 浓度不是最大值,溶液导电性就不是最大值。你认为乙学习小组的结论是否正确?________,理由是___________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com