
题目列表(包括答案和解析)




















Knoevenagel反应是有机合成中的一种常见反应:

化合物II可以由以下合成路线获得:

(1)化合物I的分子式为 。
(2)已知1mol化合物III可以与2molNa发生反应,且化合物III在Cu催化下与O2反应的产物可以被新制的Cu(OH)2氧化,则III的结构简式为 。
(3)化合物IV与NaOH醇溶液反应的化学方程式为
。IV与CH3OH生成II的反应类型为 。
(4)已知化合物V( )也能与化合物IV发生Knoevenagel反应,则其生成物的结构简式为
。
)也能与化合物IV发生Knoevenagel反应,则其生成物的结构简式为
。
(5)化合物V的一种同分异构体VI含有苯环,能发生银镜反应,同时也能发生水解,则 VI的结构简式为 (任写一种)。
(16分)Favorskii反应是化工生产中的重要反应,它是利用炔烃与羰基化合物在强碱性下发生反应,得到炔醇,反应原理为:
已知:
以下合成路线是某化工厂生产流程的一部分:
请回答下列问题:
(1)写出F中官能团的名称 。
(2)写出D的名称(系统命名) 。
(3)④的反应类型是 ;B的结构简式是 。
(4)写出反应⑥的化学方程式为 。
(5)H是D的同分异构体,核磁共振氢谱有3种峰且属于炔烃的结构简式为
、 。
(6)有关C的说法正确的是
| A.能使溴的四氯化碳溶液褪色 | B.能和氢氧化钠溶液反应 |
| C.能使酸性高锰酸钾褪色 | D.能与乙酸发生酯化反应 |
“Mannich反应”和 “付一克反应”都是有机化学中形成C―C键的重要反应。
Mannich反应: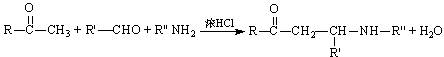
付一克反应: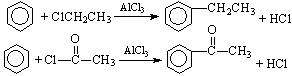
又知:![]()
已知,A在常温下为液体,1 mol A与足量O2完全燃烧所生成的CO2和H2O与足量Na2O2反应,共生成5.5 mol O2,A不能使溴水褪色,但可以使KMnO4/H+褪色,从A出发有如下图所示的转化关系,其中,F与H互为同分异构体:
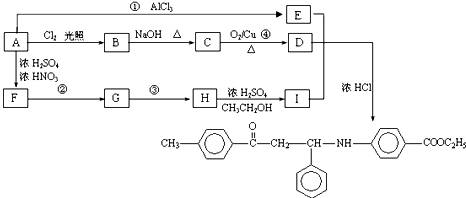
请回答下列问题:
(1)A的结构简式为_______________________________________。
(2)H中不含氧的官能团的电子式为__________________________。
(3)请判断下列反应的反应类型:①____________ ④____________
(4)反应②的试剂是________________,反应③的试剂是________________。
(5)请写出下列反应方程式:
①D与Ag(NH3)2OH溶液在水浴中反应的方程式:
______________________________________________________________________
②H在一定条件下发生缩聚反应的方程式:
_______________________________________________________________________
(6)请写出满足下列要求的I的同分异构体:
① 有苯环; ② 苯环有2个处于对位的侧链,其中一个侧链是氨基。
③ 该化合物属酯类 ④ 1mol该物质在NaOH水溶液中完全水解只消耗1mol NaOH
_________________、_______________、__________________、__________________
点评:有机合成是有机部分的重头戏,能综合考查学生对该有机基础知识掌握情况,新课标对这类题的考查特点是注重知识的广度。
猜题四 现代物理分析方法与有机结构探究相结合
例5某研究性学习小组为确定某蜡状有机物A的结构和性质,他们拟用传统实验的手段与现代技术相结合的方法进行探究。请你参与过程探究。
1、实验式的确定
(1)取样品A进行燃烧法测定。发现燃烧后只生成 ,某次燃烧后,经换算得到了
,某次燃烧后,经换算得到了 。据此得出的结论是________________________。
。据此得出的结论是________________________。
(2)另一实验中,取 蜡状A在
蜡状A在 (标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成
(标准状况下,下同)氧气中完全燃烧,两者均恰好完全反应,生成 和液态水。
和液态水。
由此得出的实验式是_____________________。
2、结构式确定(经测定A的相对分子质量为136)
(3)取少量样品熔化,加入钠有氢气放出,说明A分子中含有________基。
(4)进行核磁共振,发现只有两个特征峰,且面积比为8:4,再做红外光谱,发现与乙醇一样透过率在同一处波数被吸收。图谱如下:

则A的结构简式为______________________。
3、性质探究
(5)A的四乙酸酯在稀硫酸催化下在 中发生水解的化学方程式(产物中注明
中发生水解的化学方程式(产物中注明 )为___________________________________。
)为___________________________________。
(6)已知①

②甲醛是所有醛中还原性最强的,则合成A需要的两种醛是__________、_____________(填结构简式)
解析:样品燃烧只生成CO2和H2O,说明该有机物中一定含有C、H两种元素,可能含有O元素,结合量可以得出的结论是 (x=0、1、2…),根据
(x=0、1、2…),根据 A在
A在 (标准状况下)氧气中恰好完全燃烧,生成
(标准状况下)氧气中恰好完全燃烧,生成 和液态水。可以求出实验式为
和液态水。可以求出实验式为 。样品熔化后加入钠块有H2放出,则说明其中有羟基。由核磁共振,发现只有两个特征峰,且面积比为8:4,可以断定该有机物中的氢原子有两种,其数目之比为8:4;再由红外光谱,发现与乙醇一样透过率在同一处波数被吸收,可以断定该有机物中键的种类和醇一样;从而确定该有机物的结构简式为C(CH2OH)4。酯的水解实质是酯基断裂,碳氧单键上结合H原子,而碳氧双键上结合羟基,所以含有18的氧原子应在乙酸的羟基上。所以A的四乙酸酯在稀硫酸催化下,在
。样品熔化后加入钠块有H2放出,则说明其中有羟基。由核磁共振,发现只有两个特征峰,且面积比为8:4,可以断定该有机物中的氢原子有两种,其数目之比为8:4;再由红外光谱,发现与乙醇一样透过率在同一处波数被吸收,可以断定该有机物中键的种类和醇一样;从而确定该有机物的结构简式为C(CH2OH)4。酯的水解实质是酯基断裂,碳氧单键上结合H原子,而碳氧双键上结合羟基,所以含有18的氧原子应在乙酸的羟基上。所以A的四乙酸酯在稀硫酸催化下,在 中发生水解的化学方程式为
中发生水解的化学方程式为 ;
;
根据醛和醛加成能得到含有羟基的醛,最后再把醛基还原得到多元醇。

甲醛和乙醛以3:1进行加成得再加成H2得到C(CH2OH)4
答案:(1)分子中 ,分子式为
,分子式为
(2) (3)羟基
(3)羟基
(4)C(CH2OH)4
(5)
(6)
猜题五、化学与奥运会
例6.青海昆仑玉被定为08北京奥运会奖牌用玉,昆仑玉主要成分是由“透闪石”和“阳起石”组成的纤维状微晶结合体,透闪石(Tremolite)的化学成份为Ca2Mg5Si8O22(OH)2。下列有关说法不正确的是
A.透闪石的化学式写成氧化物的形式为:2CaO?5MgO?8SiO2?H2O
B.透闪石的化学式写成硅酸盐的形式为:2CaSiO3?5MgSiO3?H2SiO3
C.透闪石中Mg元素的质量分数是Ca元素质量分数的2倍
D.透闪石中还有少量的Al代替Mg,Na、K、Mn代替Ca、Mg等。
答案:C
解析:从化学式可知,Ca与Mg的物质的量比为2∶5,质量比为2×40∶5×24=80∶120,故质量分数比为2∶3,即Mg元素的质量分数是Ca元素的1.5倍。正确选项为C。
例7.2008年北京奥运会“祥云”奥运火炬所用环保型燃料为丙烷(C3H8),悉尼奥运会所用火炬燃料为65%丁烷(C4H10)和35%丙烷,已知:
CO:2CO(g)+O2(g)=2CO2(g),△H=-566.0 kJ/mol。
丙烷:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5 kJ/mol。
正丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l),△H=-2878.0kJ/mol。
异丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l),△H=-2869.6kJ/mol。
下列有关说法正确的是
A.常温下,正丁烷的燃烧热为-2878.0kJ/mol。
B.相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气多产生的热量也多
C.常温下,CO的燃烧热为566.0 kJ/mol。
D.人类利用的能源都是通过化学反应获得的
解析:A项中燃烧热不能带负号;B选项中等质量的烷烃,碳原子个数越多,耗氧量越低,且 ,故放出的热和消耗的氧都是前者多;C选项中566.0 kJ的热量是燃烧2 mol CO放出的热;D选项中人类利用的能源不一定是通过化学反应获得的,如风能等。故选B。
,故放出的热和消耗的氧都是前者多;C选项中566.0 kJ的热量是燃烧2 mol CO放出的热;D选项中人类利用的能源不一定是通过化学反应获得的,如风能等。故选B。
猜题六 化学与贝尔化学奖
 例8.2007年诺贝尔化学奖得主――德国科学家格哈德?埃特尔对有关一氧化碳在金属铂表面的氧化过程的研究,催生了汽车尾气净化装置。净化装置中的催化转化器, 可将CO、NO、NO2和碳氢化合物等转化无害的物质,有效降低尾气对环境的危害。下列有关说法不正确的是
例8.2007年诺贝尔化学奖得主――德国科学家格哈德?埃特尔对有关一氧化碳在金属铂表面的氧化过程的研究,催生了汽车尾气净化装置。净化装置中的催化转化器, 可将CO、NO、NO2和碳氢化合物等转化无害的物质,有效降低尾气对环境的危害。下列有关说法不正确的是
A.催化转化器中的铂催化剂可加快CO氧化
B.铂表面做成蜂窝状更有利于提高催化效果。
C. 在铂催化下,NO、NO2可被CO还原成N2
D. 碳氢化合物在铂催化下,被CO直接氧化成CO2和H2O
解析:CO是常见的还原剂,不能将碳氢化物直接氧化,碳氢化合物可直接被空气中的氧气氧化成CO2和H2O
答案:D
猜题七 化学与“嫦娥奔月”
|