
题目列表(包括答案和解析)
实验室制备少量碘乙烷:将红磷粉末放入乙醇里,在不断振荡下逐次加入细粒的I2,则有反应:
2P+3I2=2PI3
PI3+3C2H5OH→3C2H5I+H3PO3+Q(主)
PI3+3C2H5OH→(C2H5O)3P+3HI(副)
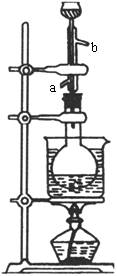
待反应缓和后用图所示装置进行水浴加热约半小时,反应可基本完成。这时反应液中已无固体颗粒I2和红磷,然后拔出直立冷凝管,加入一些物质X,装上附有60°弯玻璃管的瓶塞,并将导管接于横放的冷凝管上,水浴加热蒸馏出粗制的碘乙烷。此粗产品中混有乙醇并溶有I2(纯碘乙烷为无色难溶于水的液体,沸点为72.3℃)。
(1)(C2H5O )3P应是________有机物,写出其结构简式:________。
(2)物质X可能是________,要用它的理由是________。
(3)装置中竖直冷凝管的作用是________。冷藏水从________口进,________口出。
(4)怎样除去粗制品中的乙醇和碘?(指出加入的试剂和操作名称)
________________________。
2P+3I2=2PI3
PI3+3C2H5OH→3C2H5I+H3PO3+Q(主)
PI3+3C2H5OH→(C2H5O)3P+3HI(副)
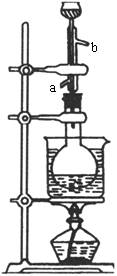
待反应缓和后用图所示装置进行水浴加热约半小时,反应可基本完成。这时反应液中已无固体颗粒I2和红磷,然后拔出直立冷凝管,加入一些物质X,装上附有60°弯玻璃管的瓶塞,并将导管接于横放的冷凝管上,水浴加热蒸馏出粗制的碘乙烷。此粗产品中混有乙醇并溶有I2(纯碘乙烷为无色难溶于水的液体,沸点为72.3℃)。
(1)(C2H5O )3P应是________有机物,写出其结构简式:________。
(2)物质X可能是________,要用它的理由是________。
(3)装置中竖直冷凝管的作用是________。冷藏水从________口进,________口出。
(4)怎样除去粗制品中的乙醇和碘?(指出加入的试剂和操作名称)
________________________。
| A、④⑤③ | B、⑥①⑤③ | C、⑧① | D、⑧②⑤③ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com