
题目列表(包括答案和解析)
下面是张家界旅游区新设的一组垃圾箱说明:
| 湖南省生活垃圾分类种类 | ||
| 可回收垃圾 | 不可回收垃圾 | 有害垃圾 |
| 纸类 玻璃 金属 塑料 橡胶 纺织品 | 厨房垃圾 灰土 杂草 枯枝 花卉 | 日光灯管 电池 喷雾罐 指甲油瓶 药品、药瓶 涂改液瓶 |
(1)小明在整理房间时,清理出如下物品,它们应分别放入哪个垃圾箱(请填序号):A.废作业本;B.汽水易拉罐;C.生锈铁钉;D.矿泉水瓶;E.烂苹果;F.涂改液瓶。
应放入“可回收垃圾箱”的是__________;
应放入“不可回收垃圾箱”的是__________;
应放入“有害垃圾箱”的是__________。
(2)小明用盐酸除去铁钉上的锈(主要成分是氧化铁),以重新使用它,请写出除锈的化学方程式______________。
(3)废铜有两种回收方法:
方法一:Cu+4HNO3===Cu(NO3)2+2X+2H2O(X是一种大气污染物)。
方法二:铜在空气中加热生成氧化铜,氧化铜再与盐酸反应生成氯化铜和水。①方法一中,X的化学式为__________,方法二的优点是__________________________。②请写出从氯化铜溶液中提取铜的化学方程式____________;该反应属于化学反应基本类型中的__________。
(4)请从可回收垃圾的类别中,举一例说说化学的研究成果给社会进步带来的贡献__________________。
(5)化学电池给人们生活带来了许多便利,但任意丢弃的一粒电池将严重污染一平方米 的土壤。一些化学成就在给人们带来方便的同时,也给人类带来危害。对此,你认为在进行化学科学研究或发明时要注意的是__________。

下列是厦门市生活垃圾分类说明:

(1)小明在整理房间时,清理出如下物品,它们应分别放入哪个垃圾箱(请填序号)
A.废作业本
B.汽水易拉罐
C.生锈铁钉
D.矿泉水瓶
E.烂苹果
F.涂改液瓶
(2)小明用盐酸除去铁钉上的锈(主要成分为氧化铁)以重新使用它,请写出除锈的化学方程式:________.
(3)废铜有两种回收方法:
方法一:Cu+4HNO3=Cu(NO3)2+2X↑+2H2O(X是一种大气污染物)
方法二:铜在空气中加热生成氧化铜,氧化铜在与盐酸反应生成氯化铜和水.
①方法一,X的化学式为________;方法二的优点是________
②请写出从氯化铜溶液中提取铜的化学方程式________;该反应属于化学反应基本类型中的________反应.
(4)请从可回收垃圾的类别中,举出一例说说化学的研究成果给社会进步带来的贡献:________.
(5)化学电池给人们生活带来许多便利,但任意丢弃的一粒电池将严重污染一平方米土壤.一些化学成就在给人们带来方便时,也给人类带来危害.对此,你认为在进行化学科学研究或发明时要注意的是:________.
1.《有机化学基础》芬必得是一种高效的消炎药,其主要成分为布洛芬,它有多种合成路线,如图就是一种合成方法。
已知卤代烃有如下反应:R—Cl+NaCN![]() R—C≡N+NaCl。
R—C≡N+NaCl。

回答下列问题:
(1)写出D的结构简式:____________________。
(2)写出反应类型:A→B____________,B→C____________。
(3)C和苯酚的关系是____________。
a.互为同分异构体 b.互为同系物
c.均为芳香族化合物 d.均属于芳香烃
(4)写出C发生消去反应的化学方程式(注明反应条件):__________________________。
(5)与A具有相同分子式,且苯环上只有一个取代基的有机物共有四种,除A的结构外,写出其余三种结构简式中的任意两种:
_____________________________、____________________________。
2.《物质结构与性质》纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。
A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 932 | 1 821 | 15 390 | 21 771 |
B | 738 | 1 451 | 7 733 | 10 540 |

(1)某同学根据上述信息,推断B的核外电子排布如上图所示,该同学所画的电子排布图违背了____________。
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为____________。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
(4)已知金刚石中的C—C的键长为154.45 pm,C60中C—C键长为145—140 pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由_________________________。
(5)科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为____________。

(6)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是__________。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为____________。
下表是元素周期的一部分,其中所列字母分别代表某一元素。
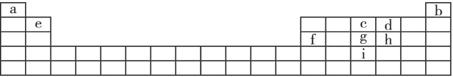
请根据表中所列a—i九种元素,回答下列问题:
(1)基态原子的价电子层中,未成对电子数最多并且原子半径最小的元素的价电子层的电子排布式________________;当此元素的原子与a元素的原子形成简单的分子时,该元素的原子杂化方式______________,所形成简单分子的立体构型为______________,该分子为______________分子(填“极性”或“非极性”)。
(2)d、g、i分别与a形成化合物,推断所形成的化合物沸点由高到低的排列顺序为______________(填化学式)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com