(2010?宝鸡二模)我国《车用燃料甲醇国家标准》的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油.甲醇可通过将煤的气化过程中生成的CO和H
2在一定条件下,发生如下反应制得:CO(g)+2H
2(g)=CH
3OH(g)
图I、图Ⅱ是关于该反应进行情况的图示.
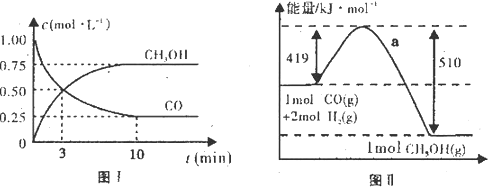
请根据图示回答下列问题:
(1)图I是反应时CO和CH
3OH的浓度随时间的变化情况,从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
0.075mol/(L?min)
0.075mol/(L?min)
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线a表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b.
(3)写出该反应的热化学方程式:
CO(g)+2H2(g)?CH3OH(g);△H=-91kJ?mol-1
CO(g)+2H2(g)?CH3OH(g);△H=-91kJ?mol-1
(4)该反应的平衡常数K的表达式为
;当温度升高时,该平衡常数K将
减小
减小
(填“增大”、“减小”或“不变”).
(5)恒容条件下,下列措施中能使
增大的有
C
C
A.升高温度 B.充入He气
C.再充入1molCO和2molH
2 D.使用催化剂.


 目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验:
目前工业上有一种方法是用CO2来生产燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol,为探究反应原理,现进行如下实验: