
题目列表(包括答案和解析)
某溶液中只可能含有下列离子中的几种(不考虑溶液中较少的H+和OH-)Na+、NH4+、SO42-、CO32-、NO3-。取200mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL。实验2:第二份先加入足量的盐酸,无现象,再加足量的BaCl2溶液,得固体2.33g。下列说法正确的是( )
A.该溶液中可能含有Na+ B.该溶液中肯定含有NH4+、S042-、CO32-、NO3-
C.该溶液中一定不含NO3- D.该溶液中一定含Na+,且c(Na+)≥0.1mol/L
下列是酸溶液与碱溶液发生反应的各种关系,请用“>”“<”或“=”填空:
(1) 取0.2 mol/LHX溶液与0.2 mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(X-)。
①混合溶液中c(HX) c(X-);
②混合溶液中c(HX) + c(X-) 0.1mol/L(忽略溶液体积变化);
③混合溶液中由水电离出的c(OH-) 0.1 mol/L 的HX溶液中由水电离出的c(H+)。
(2) 如果取0.2 mol/LHX溶液与0.1 mol/LNaOH溶液等体积混合,测得混合溶液的PH>7,则说明在相同浓度时HX的电离程度 NaX的水解程度。
(3) 分别取pH=2的硫酸和醋酸各50mL,加入足量的镁粉,反应开始时,反应速率前者_________后者;充分反应后,相同条件下产生氢气的体积前者_________后者。
(4) 等浓度等体积的盐酸和醋酸,分别与等浓度的NaOH溶液反应,恰好中和时,消耗NaOH的体积前者__________后者,所得溶液的pH前者________后者。
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 ;
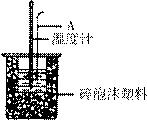 (2)如右图所示,仪器A的名称是_______________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H (填“偏大”、“偏小”或“无影响”);
(2)如右图所示,仪器A的名称是_______________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H (填“偏大”、“偏小”或“无影响”);
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g?℃)。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1℃ | 终止温度t2℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热△H=________________;(结果保留一位小数)
(4) (填“能”或“不能”)用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是 。
已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1mol?L―1的NaHSO3的溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中正确的是( )
A.c(Na+)>c(HRO3―)>c(H+)>c(RO32―)>c(OH―)
B.c(Na+)+ c(H+)=c(HRO3―)+c(RO32―)+c(OH―)
C.c(H+)+ c(HRO3―)= c(RO32―)+c(OH―)
D.两溶液中c(Na+)、c(HRO3―)、c(RO32―)分别相等
已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1mol/L-1的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中一定正确的是
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C.两溶液中c(Na+)、c(HRO3-)、c(RO32-)分别相等
D. c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com