
题目列表(包括答案和解析)
| A、蛋白质在酶的作用下水解的最终产物为氨基酸 | B、向蛋白质溶液中加入(NH4)2SO4浓溶液,会使其变性 | C、天然蛋白质仅由碳、氢、氧、氮四种元素组成 | D、氨基酸和蛋白质都是只能和碱反应的酸性物质 |
下列关于反应热的说法正确的是( )
A.在稀溶液中所有酸和碱反应的中和热数值都相等
B.已知C(s)+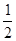 O2(g)=CO(g)
△H=-110.5kJ/mol,说明碳的燃烧热为-110.5kJ/mol
O2(g)=CO(g)
△H=-110.5kJ/mol,说明碳的燃烧热为-110.5kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com