
题目列表(包括答案和解析)
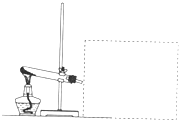 看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)
看图回答下列问题(部分仪器已被虚线遮挡,且虚线部分仪器可以根据需要添加)
| ||
| ||
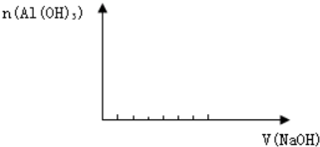
| 实验操作步骤 | 实验现象 |
1、取少量该白色粉末放入试管中,加2mL水振荡,滴加几滴无色的酚酞溶液 2、另取少量白色粉末放在试管中,滴加适量盐酸 1、取少量该白色粉末放入试管中,加2mL水振荡,滴加几滴无色的酚酞溶液 2、另取少量白色粉末放在试管中,滴加适量盐酸 |
酚酞试液变红 有气泡生成 酚酞试液变红 有气泡生成 |
| 9(b-a) |
| a |
| 9(b-a) |
| a |
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com