
题目列表(包括答案和解析)
: 关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一:“理论派”认为电解氯化铜溶液后溶液的pH升高。观点二:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH值的变化如右图曲线关系。请回答下列问题:
关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一:“理论派”认为电解氯化铜溶液后溶液的pH升高。观点二:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH值的变化如右图曲线关系。请回答下列问题:
①电解前氯化铜溶液的pH值处于A点位置的原因是: (用离子方程式说明)。
②“理论派”所持观点的理论依据是: 。
③“实验派”的实验结论是 ,他们所述“精确实验”是通过
确定的。
④你持何种观点?你所持观点的理由是(从化学原理加以简述) 。
方法:本题要从电解过程中的实际情况加以分析,即阳极产生的Cl2不能全部析出,而有部分溶于阳极区的溶液中,以此造成溶液的pH下降。
![]() 分析:①中电解前氯化铜溶液的pH值处于A点位置,显酸性,显然,其酸性的原因是CuCl2水解之故;②中“理论派”所持观点的是从电解过程中物质随着电解的进行,CuCl2溶液的浓度下降,造成Cu2+水解产生的H+浓度下降。③中实验派的实验结论可从图示找得答案,随电解的进行,酸性增强。④回答个人所持观点,应尊重实验事实,从实验的实际情况出发,以此可得解题结果。
分析:①中电解前氯化铜溶液的pH值处于A点位置,显酸性,显然,其酸性的原因是CuCl2水解之故;②中“理论派”所持观点的是从电解过程中物质随着电解的进行,CuCl2溶液的浓度下降,造成Cu2+水解产生的H+浓度下降。③中实验派的实验结论可从图示找得答案,随电解的进行,酸性增强。④回答个人所持观点,应尊重实验事实,从实验的实际情况出发,以此可得解题结果。
①2KClO3+2MnO2![]() 2A+B↑+C↑
2A+B↑+C↑
②2A![]() D+MnO2+C↑;
D+MnO2+C↑;
③B+D![]() 2KCl+MnO2+C↑
2KCl+MnO2+C↑
试判断:
(1)氯酸钾分解的总反应方程式:________________________________________;
(2)反应①中的氧化剂是____________________;
(3)反应③的化学方程式为:____________________________________________;
(4)按上述反应过程,若要制取1.5 mol氧气,总共有________mol电子转移。
研究物质性质的基本程序
1.研究物质性质的基本程序
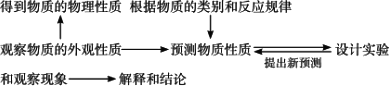
2.研究氯气的性质
(1)认识Cl2的物理性质
(2)Cl2的化学性质

(3)氯水的性质

(4)含氯化合物的漂白与消毒作用
①HClO不仅有漂白作用,还有杀菌消毒作用.次氯酸盐是常用漂白剂和消毒剂的主要成分.
2NaOH+Cl2![]() NaCl+NaClO+H2O
NaCl+NaClO+H2O
NaClO+H2O+CO2![]() NaHCO3+HClO
NaHCO3+HClO
②漂白粉的制取原理
2Ca(OH)2+2Cl2![]() CaCl2+Ca(ClO)2+2H2O
CaCl2+Ca(ClO)2+2H2O
漂白粉的失效:在空气中放置过长,就会与空气中的CO2及水蒸气反应生成HClO,HClO分解,就会导致漂白粉失效.
Ca(ClO)2+CO2+H2O![]() CaCO3↓+2HClO,2HClO
CaCO3↓+2HClO,2HClO![]() 2HCl+O2↑
2HCl+O2↑
(5)假说和模型
①假说:是以已有事实材料和科学理论为依据,面对未知事实或规律所提出的一种推测性说明.
②模型:是以客观事实为依据建立起来的,是对事物及其变化的简单模拟.
(6)现代化学实验室
①先进的新型仪器:色谱仪、质谱仪等.
②计算机化学:用计算机做实验.
在氯酸钾的分解反应中,关于二氧化锰的催化问题,到目前还没有明确的解释.鉴于反应制得的氧气中有氯气的气味,生成的氯化钾又略带紫红色的客观事实,一种分析认为其反应过程如下:
①2KClO3+2MnO2![]() 2A+B↑+C↑
2A+B↑+C↑
②2A![]() D+MnO2+C↑
D+MnO2+C↑
③B+D![]() 2KCl+MnO2+C↑
2KCl+MnO2+C↑
试判断:
(1)氯酸钾分解的总反应方程式:_______________.
(2)反应①中的氧化剂是_______________________.
(3)反应③的化学方程式为_____________________.
(4)按上述反应过程,若要制取1.5 mol氧气,总共有________mol电子转移.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com