
题目列表(包括答案和解析)
 有些化学反应的化学能能直接转化成电能
有些化学反应的化学能能直接转化成电能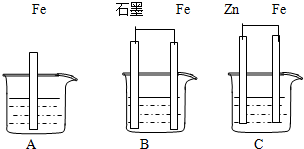
| 放电 | 充电 |


生成沉淀的离子反应之所以能够发生,在于生成物的溶解度________AgCl的溶解度仅为1.5×10-4 g。尽管生成物的溶解度________,但并不是绝对________ ,生成的沉淀物会有________。因此生成沉淀后的溶液中有关反应的粒子在反应体系中________。如生成AgCl沉淀后溶液中有关反应的粒子在体系中共存:______________。
从固体溶解平衡的角度可以理解AgCl在溶液中存在下述两个过程:一方面,在水分子作用下,少量________脱离AgCl的表面________水中;另一方面,溶液中的离子受AgCl表面正、负离子的吸引,回到AgCl的表面析出——________。
(1)溶解平衡:在一定温度下,当________和________的速率相等时,即达到溶解平衡状态。如AgCl沉淀体系中的溶解平衡可表示为_____________。由于沉淀、溶解之间的这种动态平衡的存在,决定了Ag+和Cl-的反应________进行到底。
(2)不同电解质在水中的溶解度差别________,但难溶电解质与易溶电解质之间并无严格界限,习惯上将溶解度小于________g的电解质称为难溶电解质。
对于常量的化学反应来说,0.1 g是很小的,因此一般情况下,相当量的离子互相反应生成难溶电解质,可以认为反应完全了。
化学上通常认为残留在溶液中的离子浓度小于________时,沉淀就达完全。
有些化学反应的化学能能直接转化成电能
I.利用 Fe + CuSO4 = FeSO4 + Cu反应,设计一个原电池:
(1)在下框中画出装置图(标明电解质溶液、正、负极和电极材料)

(2)下列说法中,正确的是 。(填字母)
A.电解质溶液中阳离子向负极移动 B.电子通过外导线由负极流向正极
C.当导线中有1mol电子通过时,理论上正极放出1g气体
D.若所选电极的质量相等,理论上两极质量差为60g,导线中有1 mol电子通过
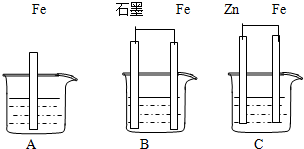
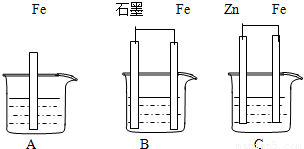
II.三套装置如下图所示, A、B、C烧杯中分别盛有相同物质的量浓度的稀硫酸。
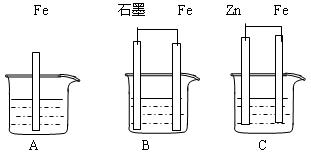
(1)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为 ;
(2)若C中电解质溶液是氯化钠溶液,则Fe电极的电极反应式为 ;
III.目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
![]()
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸。
(1)以下说法中正确的是
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
(2)废弃的镍镉电池已成为重要的环境污染物,资料表明一节废镍镉电池可以使一平方米面积的耕地失去作用价值。在酸性土壤中这种污染特别严重,这是因为
(3)另一种常用的电池是锂电池,锂是一种碱金属元素,其相对原子质量为7,由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年,它的负极用金属锂制成,电池总反应可表示为Li+ MnO2 = LiMnO2。
锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液(请用化学方程式表示其原因) 。
 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com