
题目列表(包括答案和解析)
| 族 周期 |
ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | |||||


| ||
| ||
(12分)材料(选修三课本第44页实验2-2):向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
![]() Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出与H2O分子互为等电子体的微粒 (填2种)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是 。
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
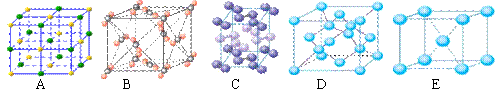
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是 (请用相应的编号填写)。
Ⅱ.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上。
(4) 写出铜原子价电子层的电子排布式 ,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有 (填元素符号)。
(5) 实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有 。
(6) 实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是 。
有A、B、C、D、W五种元素。W的原子序数为29,其余的均为短周期主族元素;其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B元素氢化物与其最高价氧化物对应水化物之间反应生成一种盐;C原子最外层中有两个未成对的电子;D原子核内的质子数与中子数相等,能与C形成DC2、DC3常见化合物。根据以上条件,回答下列问题:
(1)推断元素名称:A 。
(2)B元素的氢化物的空间构型为 ,分子中的化学键 (填“有”或“无”)极性,其分子为 分子(填“极性”或“非极性”)。
(3)比较A、B、C三种元素的第一电离能由小到大的顺序 (用元素符号表示),A、B、C三种元素的氢化物的沸点由高到低的顺序 (用化学式表示)。
(4)写出D元素原子基态时的电子排布式 ,其在元素周期表中的位置 。
(5)W元素+2价离子的水溶液呈现天蓝色,是该离子与水分子通过 键形成的 (填化学式)而显示出的颜色,在W元素+2价离子的水溶液中滴加氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,得到配位数为4的的配合物。写出沉淀溶解的离子方程式 。
材料(选修三课本第44页实验2-2):向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体.
(Ⅰ)在化学实验和科学研究中,水是一种最常用的溶剂.水是生命之源,它与我们的生活密切相关.
(1)写出与H2O分子互为等电子体的微粒________(填1种).
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是________.
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为________
(Ⅱ)胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上.
(4)写出铜原子价电子层的电子排布式________,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有________(填元素符号).
(5)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;以上过程中发生的离子反应方程式为:________;________.
实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有________.
(6)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体.实验中所加C2H5OH的作用是________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com