
题目列表(包括答案和解析)
(16分)向一定体积的密闭器中加入2 mol A、0.6 mo1 C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图(Ⅰ)所示,其中t0~t1 阶段c(B)未画出.图(Ⅱ)为t2时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中t3~t4阶段为使用催化剂.
请回答下列问题:
(1)若t1=15 min,则t0~t1阶段以C物质的浓度变化表示反应速率为 。
(2) t4~t5阶段改变的条件为 ,B的起始物质的量浓度为 ,各阶段平衡时对应的平衡常数如下表所示:
| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
则K1= (保留两位小数),
K1、K2、K3、K4、K5之间的关系为 (用“>”、“<”或“=”连接).
(3) t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式
。
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为 .
【解析】(1)化学反应速率通常用单位时间内浓度的变化量来表示。根据图像I可知在15min内C的浓度变化量是0.6mol/L-0.3mol/L=0.3mol/L,所以速率为
(2)由图像Ⅱ可知,在t4~t5阶段反应速率减小,但平衡不移动,所以改变的条件不可能是温度和浓度,由于在t3~t4阶段为使用催化剂,所以该阶段只是降低压强。这说明改变压强平衡不移动,因此反应前后体积是不变的。根据图像I可知A是反应物,C是生成物,二者的变化量之比是2︰3,所以要使反应前后体积不变,B只是反应物,及反应的方程式为2A+B3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为
![]() 。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
(3)根据题意科判断,每消耗0.01molA,反应就吸收能量akJ,所以反应的热化学方程式为2A(g)+B(g)⇋3C(g) △H=+200kJ/mol。
(4)因为容器容积不变(容器容积是2L),所以要使平衡等效,则起始物质的物质的量是相等的。根据题意可知起始时AB的物质的量分别为2.4mol和1.2mol,则把cmol的C转化为AB,则AB的物质的量(mol)分别是a+2c/3、b+c/3,所以关系式必须满足a+2c/3=2.4、b+c/3=1.2.
(12分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g);ΔH
(1)已知,该反应在300℃,5MPa条件下能自发进行,则ΔH 0,△S 0 (填“<,>或=”)。
(2)在300℃,5MPa条件下,将0.20mol的 CO与0.58mol H2的混合气体充入2L密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示。
①在0~2min内,以H2表示的平均反应速率为 mol·L-1·s-1。
②列式计算300℃时该反应的平衡常数K = 。
③300℃时,将0.50mol CO、1.00mol H2和1.00 molCH3OH充入容积为2L的密闭容器中,此时反应将 。
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
④下列措施可增加甲醇产率的是
A.压缩容器体积 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入0.20mol CO和0.58mol H2
(3)若其它条件不变,使反应在500℃下进行,在图中作出甲醇的物质的量浓度随时间的变化的示意图。
【解析】(1)根据反应的特点可知△S小于0,因为反应在300℃,5MPa条件下能自发进行,所以根据△G=△H-T·△S可知反应是放热反应。
(2)①反应速率通常用单位时间内浓度的变化量来表示,根据图像可知反应进行到2min时甲醇
的浓度不再发生变化,平衡时甲醇的物质的量是0.04mol,则消耗氢气是0.08mol,所以在0~2min
内,以H2表示的平均反应速率为![]() 。
。
②平衡时氢气的浓度是![]() ,CO的平衡浓度是
,CO的平衡浓度是
![]() ,所以该温度下的平衡常数为
,所以该温度下的平衡常数为![]() 。
。
③300℃时,将0.50mol CO、1.00mol H2和1.00 molCH3OH充入容积为2L的密闭容器中,此时它们的浓度分别为0.25mol/L、0.50mol/L、、0.50mol/L,因为![]() >4,所以反应向逆反应方向移动。
>4,所以反应向逆反应方向移动。
④压缩体积,压强增大,平衡向正反应方向移动。选项B是降低生成物浓度,平衡也向正反应方
向移动。充入He,使体系总压强增大,但物质但浓度没有变化,所以平衡不移动。再充入0.20mol
CO和0.58mol H2,相当于增大体系的压强,平衡向正反应方向移动,所以答案是ABD。
(3)因为反应是放热反应,所以升高温度平衡向逆反应方向移动,但反应速率会加快,所以图
像为
(16分) 向一定体积的密闭器中加入2 mol A、0.6 mo1 C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图(Ⅰ)所示,其中t0~t1 阶段c(B)未画出.图(Ⅱ)为t2时刻后改变反应条件,化学反应速率随时间变化的情况,四个阶段改变的条件均不相同,每个阶段只改变浓度、温度、压强、催化剂中的一个条件,其中t3~t4阶段为使用催化剂.

请回答下列问题:
(1)若t1=15 min,则t0~t1阶段以C物质的浓度变化表示反应速率为 。
(2) t4~t5阶段改变的条件为 ,B的起始物质的量浓度为 ,各阶段平衡时对应的平衡常数如下表所示:
|
t1~t2 |
t2~t3 |
t3~t4 |
t4~t5 |
t5~t6 |
|
K1 |
K2 |
K3 |
K4 |
K5 |
则K1= (保留两位小数),
K1、K2、K3、K4、K5之间的关系为 (用“>”、“<”或“=”连接).
(3) t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01 mol,而此过程中容器与外界的热交换总量为akJ,写出此温度下该反应的热化学方程式
。
(4)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为 .
【解析】(1)化学反应速率通常用单位时间内浓度的变化量来表示。根据图像I可知在15min内C的浓度变化量是0.6mol/L-0.3mol/L=0.3mol/L,所以速率为
(2)由图像Ⅱ可知,在t4~t5阶段反应速率减小,但平衡不移动,所以改变的条件不可能是温度和浓度,由于在t3~t4阶段为使用催化剂,所以该阶段只是降低压强。这说明改变压强平衡不移动,因此反应前后体积是不变的。根据图像I可知A是反应物,C是生成物,二者的变化量之比是2︰3,所以要使反应前后体积不变,B只是反应物,及反应的方程式为2A+B 3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为
3C。C的浓度增加了0.3mol/L,则B的浓度减少了0.1mol/L,所以B的起始浓度是0.4mol/L+0.1mol/L=0.5mol/L。在t1~t2阶段平衡是ABC的浓度(mol/L)分别为0.8、0.4、0.6,所以平衡常数为 。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
。因为平衡常数只与温度有关,根据图像可知在t5~t6阶段,正逆反应速率同时增大,但平衡向正反应方向移动,因为该条件只能是温度且是升高温度,所以反应是吸热反应,因此K1、K2、K3、K4、K5之间的关系为K1=K2=K3=K4<K5。
(3)根据题意科判断,每消耗0.01molA,反应就吸收能量akJ,所以反应的热化学方程式为2A(g)+B(g)⇋3C(g) △H=+200kJ/mol。
(4)因为容器容积不变(容器容积是2L),所以要使平衡等效,则起始物质的物质的量是相等的。根据题意可知起始时AB的物质的量分别为2.4mol和1.2mol,则把cmol的C转化为AB,则AB的物质的量(mol)分别是a+2c/3、b+c/3,所以关系式必须满足a+2c/3=2.4、b+c/3=1.2.
(12分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g);ΔH
CH3OH(g);ΔH
(1)已知,该反应在300℃,5MPa条件下能自发进行,则ΔH 0,△S 0 (填“<,>或=”)。
(2)在300℃,5MPa条件下,将0.20mol的 CO与0.58mol H2的混合气体充入2L密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示。

①在0~2min内,以H2表示的平均反应速率为 mol·L-1·s-1 。
②列式计算300℃时该反应的平衡常数K = 。
③300℃时,将0.50mol CO、1.00mol H2和1.00 mol CH3OH充入容积为2L的密闭容器中,此时反应将 。
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
④下列措施可增加甲醇产率的是
A.压缩容器体积 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入0.20mol CO和0.58mol H2
(3)若其它条件不变,使反应在500℃下进行,在图中作出甲醇的物质的量浓度随时间的变化的示意图。
【解析】(1)根据反应的特点可知△S小于0,因为反应在300℃,5MPa条件下能自发进行,所以根据△G=△H-T·△S可知反应是放热反应。
(2)①反应速率通常用单位时间内浓度的变化量来表示,根据图像可知反应进行到2min时甲醇
的浓度不再发生变化,平衡时甲醇的物质的量是0.04mol,则消耗氢气是0.08mol,所以在0~2min
内,以H2表示的平均反应速率为 。
。
②平衡时氢气的浓度是 ,CO的平衡浓度是
,CO的平衡浓度是
 ,所以该温度下的平衡常数为
,所以该温度下的平衡常数为 。
。
③300℃时,将0.50mol CO、1.00mol H2和1.00 mol
CH3OH充入容积为2L的密闭容器中,此时它们的浓度分别为0.25mol/L、0.50mol/L、、0.50mol/L,因为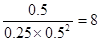 >4,所以反应向逆反应方向移动。
>4,所以反应向逆反应方向移动。
④压缩体积,压强增大,平衡向正反应方向移动。选项B是降低生成物浓度,平衡也向正反应方
向移动。充入He,使体系总压强增大,但物质但浓度没有变化,所以平衡不移动。再充入0.20mol
CO和0.58mol H2,相当于增大体系的压强,平衡向正反应方向移动,所以答案是ABD。
(3)因为反应是放热反应,所以升高温度平衡向逆反应方向移动,但反应速率会加快,所以图
像为

(4分)下列反应在210℃时达到平衡:
①PCl5(g) PCl3(g)+Cl2(g);
△H1>0 K1=10
PCl3(g)+Cl2(g);
△H1>0 K1=10
②CO(g)+Cl2(g) COCl2(g);△H1<0 K2= 5×103
COCl2(g);△H1<0 K2= 5×103
③PCl5(g) +CO(g) COCl2(g) + PCl3(g)
K3
COCl2(g) + PCl3(g)
K3
(1)反应③的平衡常数K3 = 。
(2)要使反应①和反应②的K数值相等,可采取的措施是 (填序号)。
A.降低反应①、②体系中Cl2浓度 B.反应①、②选择不同的催化剂
C.反应①、反应②同时升高温度 D.降低反应①、反应②的体系压强
E.反应①降低温度,反应②维持210℃
【解析】当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值称作平衡常数。①+②即得到③,所以③的平衡常数为10×5×103= 5×104.。反应①是吸热反应,②是放热反应,所以要使反应①和反应②的K数值相等,则反应①要向正反应方向移动,反应②要向逆反应方向移动,所以答案是C。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com