ЃЈ2008?дцзЏвЛФЃЃЉШМСЯКЭФмдДЪЧЛЏбЇжЊЪЖгыЩчЛсЩњЛюСЊЯЕМЋЮЊУмЧаЕФФкШнЃЎЮвУЧвЊЙизЂПѓЮяФмдДЕФКЯРэРћгУЃЌЛ§МЋбаОПЁЂПЊЗЂаТФмдДЃЎ
ЃЈ1ЃЉаТФмдДгІИУОпгадзДСЯвзЕУЁЂШМЩеЪБВњЩњЕФШШСПЖрЧвВЛЛсЮлШОЛЗОГЬиЕуЃЎдкУКЬПЁЂЪЏгЭЁЂУКЦјЁЂЧтЦјжаЃЌЧАЭОЙуРЋЕФФмдДЪЧ
ЧтЦј
ЧтЦј
ЃЎ
ЃЈ2ЃЉНќФъРДЃЌЮвЙњУКПѓЪТЙЪДѓЖрЪЧгЩгкЭпЫЙБЉеЈЫљжТЃЎЭпЫЙжаКЌгаМзЭщКЭвЛбѕЛЏЬМЕШЦјЬхЃЌЕБПѓОЎжаЭпЫЙХЈЖШДяЕНвЛвЛЖЈЗЖЮЇЪБгіУїЛ№МДШМЩеБЌеЈЃЎЮЊБмУтджФбЕФЗЂЩњгІВЩШЁЕФЧаЪЕПЩааЕФДыЪЉга
ЂйЂл
ЂйЂл
ЃЈЬюађКХЃЉ
ЂйМгЧПАВШЋЙмРэЃЌЖХОјУїЛ№дД
ЂкНЕЕЭЭпЫЙЦјЬхЕФзХЛ№Еу
ЂлЬсИпЭЈЗчФмСІЂмНЋПѓОЎжаЕФбѕЦјГщШЅ
ЃЈ3ЃЉЮЊСЫЬсИпУКЕФШШаЇгІЃЌЭЌЪБМѕЩйШМЩеЪБЕФЛЗОГЮлШОЃЌГЃНЋУКзЊЛЏЮЊЫЎУКЦјЃЌетЪЧНЋУКзЊЛЏЮЊНрОЛШМСЯЕФЗНЗЈжЎвЛЃЎЫЎУКЦјЕФжївЊГЩЗжЪЧвЛбѕЛЏЬМЕФЧтЦјЃЌЫќЪЧгЩУКЬПКЭЫЎеєЦјЗДгІжЦЕУЃЌвбжЊCЃЈЪЏФЋЃЉЁЂCOЁЂH
2ШМЩеЕФШШЛЏбЇЗНГЬЪНЮЊЃК
CЃЈsЃЌЪЏФЋЃЉ+O
2ЃЈgЃЉЈTCO
2ЃЈgЃЉЃЌЁїH
1=-393.5kJ?mol
-1H
2ЃЈgЃЉ+
O
2ЃЈgЃЉЈTH
2OЃЈgЃЉЃЌЁїH
2=-241.8kJ?mol
-1COЃЈgЃЉ+O
2ЃЈgЃЉЈTCO
2ЃЈgЃЉЃЌЁїH
3=-283.0kJ?mol
-1H
2ЃЈgЃЉ+
O
2ЃЈgЃЉЈTH
2OЃЈlЃЉЃЌЁїH
4=-285.8kJ?mol
-1ЧыЛиД№ЯТСаЮЪЬтЃК
ЂйИљОнЩЯЪіЬсЙЉЕФШШЛЏбЇЗНГЬЪНМЦЫуЃЌ36gЫЎгЩвКЬЌБфГЩЦјЬЌЕФШШСПБфЛЏЪЧ
ЮќЪе88kJ
ЮќЪе88kJ
ЃЎ
ЂкаДГіCЃЈsЃЌЪЏФЋЃЉгыЫЎеєЦјЗДгІЕФШШЛЏбЇЗНГЬЪН
CЃЈsЃЌЪЏФЋЃЉ+H2OЃЈgЃЉ=COЃЈgЃЉ+H2ЃЈgЃЉЁїH=+131.3kJ?mol-1
CЃЈsЃЌЪЏФЋЃЉ+H2OЃЈgЃЉ=COЃЈgЃЉ+H2ЃЈgЃЉЁїH=+131.3kJ?mol-1
ЃЎ
ЂлБћЭщЪЧвКЛЏЪЏгЭЦјЕФжївЊГЩЗжжЎвЛЃЌБћЭщШМЩеЕФШШЛЏбЇЗНГЬЪНЮЊЃК
C
3H
8ЃЈgЃЉ+5O
2ЃЈgЃЉЈT3CO
2ЃЈgЃЉ+4H
2OЃЈgЃЉЃЌЁїH=-2220.0kJ?mol
-1ЯрЭЌЮяжЪЕФСПЕФБћЭщКЭвЛбѕЛЏЬМЭъШЋШМЩеЩњГЩЦјЬЌВњЮяЪБЃЌВњЩњЕФШШСПжЎБШЮЊ
2220ЃК283
2220ЃК283
ЃЛЯрЭЌжЪСПЕФЧтЦјКЭБћЭщЭъШЋШМЩеЩњГЩЦјЬЌВњЮяЪБЃЌВњЩњЕФШШСПжЎБШЮЊ
5319.6ЃК2220
5319.6ЃК2220
ЃЎ

 ФГЗМЯуЬўXЪЧвЛжжживЊЕФгаЛњЛЏЙЄдСЯЃЌЫќЕФЯрЖдЗжзгжЪСПЮЊ92ЃЎбаОПВПУХвдXЮЊГѕЪМдСЯЩшМЦГіШчЯТзЊЛЏЙиЯЕЭМЃЈВПЗжВњЮяЁЂКЯГЩТЗЯпЁЂЗДгІЬѕМўТдШЅЃЉЃЌЦфжаAЪЧвЛТШДњЮяЃЌHЪЧвЛжжЙІФмИпЗжзгЃЌСДНкзщГЩЮЊC7H5NOЃЎ
ФГЗМЯуЬўXЪЧвЛжжживЊЕФгаЛњЛЏЙЄдСЯЃЌЫќЕФЯрЖдЗжзгжЪСПЮЊ92ЃЎбаОПВПУХвдXЮЊГѕЪМдСЯЩшМЦГіШчЯТзЊЛЏЙиЯЕЭМЃЈВПЗжВњЮяЁЂКЯГЩТЗЯпЁЂЗДгІЬѕМўТдШЅЃЉЃЌЦфжаAЪЧвЛТШДњЮяЃЌHЪЧвЛжжЙІФмИпЗжзгЃЌСДНкзщГЩЮЊC7H5NOЃЎ
 ЃЈБНАЗЃЌвзБЛбѕЛЏЃЉ
ЃЈБНАЗЃЌвзБЛбѕЛЏЃЉ





 КЭЦфЫћЮоЛњЮяКЯГЩ
КЭЦфЫћЮоЛњЮяКЯГЩ ЩшМЦзюКЯРэЕФЗНАИЃЌаДГіКЯГЩТЗЯпЃЈашзЂУїЗДгІЬѕМўЃЉ
ЩшМЦзюКЯРэЕФЗНАИЃЌаДГіКЯГЩТЗЯпЃЈашзЂУїЗДгІЬѕМўЃЉ


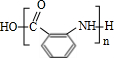



 гаЖржжЭЌЗжвьЙЙЬхЃЌЦфжаКЌга1ИіШЉЛљКЭ2ИієЧЛљЕФЗМЯузхЛЏКЯЮяЙВга
гаЖржжЭЌЗжвьЙЙЬхЃЌЦфжаКЌга1ИіШЉЛљКЭ2ИієЧЛљЕФЗМЯузхЛЏКЯЮяЙВга зюКЯРэЕФЗНАИЃЈВЛГЌЙ§4ВНЃЉЃЎ
зюКЯРэЕФЗНАИЃЈВЛГЌЙ§4ВНЃЉЃЎ






 ЃЈЫЎбюЫсЃЉгаЖржжЭЌЗжвьЙЙЬхЃЌаДГіШЮвтвЛжжЗћКЯЯТСаЬѕМўЕФНсЙЙМђЪН
ЃЈЫЎбюЫсЃЉгаЖржжЭЌЗжвьЙЙЬхЃЌаДГіШЮвтвЛжжЗћКЯЯТСаЬѕМўЕФНсЙЙМђЪН
