研究铁及铁的化合物的性质具有重要意义.
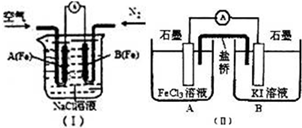
(1)如图(I)是为研究钢铁腐蚀部位与水中O
2浓度的关系而设计的装置,该装置化学上称为差异充气电池.实验中观察到电流计指针偏转,B(Fe)极被腐蚀,则A(Fe)极的电极反应式为
.
(2)常温下,铁可在某些强氧化剂溶液中形成钝化膜而被保护.为探究钝化膜的成分,取一小段钝化后的铁片放入稀硫酸中加热,使铁片完全溶解.取1mL溶解液滴入3~5滴KmnO
4溶液,观察到溶液紫色逐渐退去,则该反应的离子方程式是
;另取1mL溶解滴入3~5滴KSCN溶液,发现溶液不变色.能否由此推断钝化膜中不含+3价的铁?
(填“能”或“不能”),理由是
(用离子方程式表示).
(3)FeC1
3溶液与KI溶液混合,离子方程式为
.若要证明该反应为逆反应,某同学设计如下方法:
[方法1]取2mL0.1mol?L
-1
溶液(填化学式)于试管中,然后加入0.5mL0.1mol?L
-1
溶液(填化学式),充分振荡后,将混合液分成两份.一份加入
溶液(填化学式),若溶液变红色;另一份加入
溶液(填化学式),若溶液变蓝色,证明该反应为可逆反应.
[方法2]设计原电池装置如图(II),测得电流计指针偏转方向是电子的流动方向.开始观察到电流计指针向
(填“A”或“B”)集团,一段时间后,电流计指针不再偏转.此时若要证明电池反应达到平衡状态,可采取的方法及观察到的现象为
.


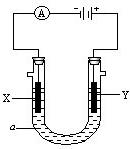 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解 液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解 液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: 研究铁及铁的化合物的性质具有重要意义.
研究铁及铁的化合物的性质具有重要意义. Ⅰ山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池.
Ⅰ山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池.