
题目列表(包括答案和解析)
【潍坊市2009届3月份高考模拟化学】下列说法正确的是【 】
A.淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体
B.从形式上看,酯化反应也属于取代反应
C.油脂的相对分子质量都较大,所以属于高分子化合物
D.乙烯能使酸性高锰酸钾溶液和溴水褪色,二者反应原理相同
(浙江舟山中学2009届度第一学期高三期中考试,化学,24)某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,下图是测定装置的示意图,A中的试剂是盐酸。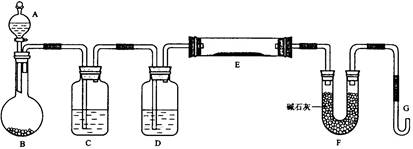
请回答下列问题。
(1)仪器中装入的试剂:B_________ 、C________、D___________;
(2)连接好装置后应首先_________________________;
(3)“加热反应管E”和“从A瓶逐滴滴加液体”这两步操作应该先进行的是:
____________________。在这两步之间还应进行的操作是_____________________;
(4)反应过程中G管逸出的气体是________________,其处理方法是:
______________________________________________________________________。
(5)从实验中测得了下列数据
①空E管的质量a
②E管和WO3的总质量b
③反应后E管和W粉的总质量c(冷却到室温称量)
④反应前F管及内盛物的总质量d
⑤反应后F管及内盛物的总质量e
由以上数据可以列出计算W的相对原子质量的两个不同计算式(除W外,其他涉及的元素的相对原子质量均为已知):
计算式1:Ar(W)=____________;计算式2:Ar(W)=____________。
(江苏省2009届高三化学各地名校月考)工业上目前使用两种方法制取乙醛:(1)乙炔水化法;(2)乙烯氧化法。下列两表提供生产过程中原料、反应条件、原料平衡转化率、产量等有关的信息情况:
表一:原料、反应条件、平衡转化率、日产量
| 乙炔水化法 | 乙烯氧化法 | |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4、100~125℃ | PdCl2-CuCl2、100~125℃ |
| 平衡转化率 | 乙炔平衡转化率90%左右 | 乙烯平衡转化率80%左右 |
| 日产量 | 2.5吨(某设备条件下) | 3.6吨(相同设备条件下) |
表二:原料来源生产工艺
| 原料生产工艺过程 | |
| 乙炔 |
|
| 乙烯 | 来源于石油裂解气 |
根据上述两表,回答下列问题:
(1)从两表中分析,现代工业上乙烯氧化法逐步取代乙炔水化法(从环境、原料来源、产率和产量、能耗等角度),分析可能的原因。
(2)若乙烯由石油裂化(裂化气混合气体的平均化学式CnHm、m>2n),进一步完全催化裂解而来,得到体积百分含量分别为:甲烷:5%、乙烯:40%、丙烯:10%、其余为丁二烯和氢气(气体体积均在同温同压下测定)。若得到40mol乙烯,求:能够得到丁二烯和氢气的物质的量各为多少?
(福建省漳州市芗城中学2009届高三一轮复习单元测试,化学,3)实验室配制1mol·L-1盐酸250mL,下列不需用的仪器是
A.250 mL容量瓶 B.托盘天平 C.胶头滴管 D.烧杯
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com