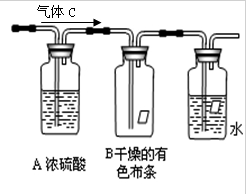
(一)某同学应用如下所示装置研究物质的性质.其中气体A的主要成分是氯气,还含有少量空气和水蒸气.请回答下列问题:

(1)浓硫酸的作用是
除去氯气中的水蒸气
除去氯气中的水蒸气
.
(2)B中观察到的实验现象是
不褪色
不褪色
.
(3)从物质性质方面来看,这样的实验设计还存在事故隐患,应如何处理,请画出装置图(填在上图内),用化学方程式表达原理
Cl2+2NaOH=NaCl+NaClO+H2O
Cl2+2NaOH=NaCl+NaClO+H2O
(二)新制的氯水含有的分子和离子,现分别做如下实验:
将紫色石蕊试液滴入,溶液显红色,起作用的微粒是
H+
H+
.上述溶液逐渐褪去,起作用的微粒是
HClO
HClO
.
加入AgNO
3溶液,有不溶于稀硝酸的白色沉淀生成,起作用的微粒是
Cl-
Cl-
.
(三)在标准状况下,35.5g氯气的体积是
11.2
11.2
L,将其与氢气完全化合,需氢气的物质的量是
0.5
0.5
mol,将生成的气体制成1L溶液,溶质的物质的量浓度是
1
1
mol?L-1,将此溶液取出20mL加蒸馏水稀释成200mL溶液,此稀稀后的溶液中溶质的物质的量浓度是
0.1
0.1
mol?L-1.