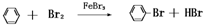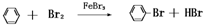实验室用图装置制取少量溴苯,回答下列问题.
(1)在烧瓶a中装的试剂是
苯、溴、三溴化铁
苯、溴、三溴化铁
,反应的化学方程式是
.
(2)跟烧瓶口垂直的一段长导管的作用是
导气和冷凝反应物的作用;
导气和冷凝反应物的作用;
.
(3)C中盛放CCl
4的作用是
吸收HBr中的溴蒸汽
吸收HBr中的溴蒸汽
.
(4)生成的溴苯因溶有未反应的溴而显褐色,提纯的方法是
将溶有溴的溴苯倒入盛有NaOH溶液的烧杯中,振荡,溴苯的密度大于水,沉在下层,用分液漏斗分离出溴苯.
将溶有溴的溴苯倒入盛有NaOH溶液的烧杯中,振荡,溴苯的密度大于水,沉在下层,用分液漏斗分离出溴苯.
.
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向锥形瓶C中加入AgNO
3溶液,若
生成淡黄色沉淀
生成淡黄色沉淀
,则能证明.另一种验证的方法是向锥形瓶C中加入
石蕊试液
石蕊试液
,现象是
溶液变红色.
溶液变红色.
.
(6)实验结束时,将氢氧化钠溶液倒入烧瓶中,充分振荡,目的是
除去溶于溴苯中的溴
除去溶于溴苯中的溴
,写出有关的化学方程式
Br2+2NaOH=NaBr+NaBrO+H2O
Br2+2NaOH=NaBr+NaBrO+H2O
.

 实验室用图装置制取少量溴苯,回答下列问题.
实验室用图装置制取少量溴苯,回答下列问题.