
题目列表(包括答案和解析)

【10福建宁德13】.(15分)
(1)(4分)乳酸亚铁片可用于治疗缺铁性贫血。右图为乳酸亚铁说明书上部分文字。请仔细阅读后回答以下问题:
①乳酸亚铁中含有 种元素。
②乳酸亚铁中碳、铁两种元素的质量比为 。
③服药时不能喝茶的原因是 。
(2)(5分)下表是元素周期表的一部分,请你根据下表回答问题:
| 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 29.95 |
①钠的相对原子质量是 。
②上表中,金属元素有 种。
③食盐的主要成分是 (填化学式)。
(3)(6分)今年西南的持久旱灾牵动全国人民的心,灾区饮水安全成为人们关注的重要问题。请你应用以下资料及所学的化学知识,为灾区人民提供饮水安全常识。
【资料在线】我国生活饮用水的标准:
| 感官指标 | 化学指标 | 细菌指标 |
| 水质无色无味 且澄清透明 | pH6.5~8.5;总硬度<250mg/L (以碳酸钙计);铜<1.0mg/L;……等 | 细菌总数<100个/mL等 |
①为了使灾区饮用水达到感官指标中的任意一项要求,可采用的净水方法有 (写一种方法即可)。
②检验灾区某水样是硬水还是软水,常用的物质是 。
③漂白粉可用于饮用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2],次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为 。
④爱护水资源,人人有责。作为中学生,在日常生活中,你的节水方法是
(写一种方法即可)。

(15分)现有实验室制取气体的部分装置,请结合所学化学知识,回答有关问题: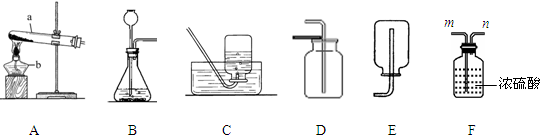
(1)请写出图中标有字母的仪器名称:a为 、b为 。
(2)实验室用高锰酸钾制取氧气,为了防止固体粉末随气流吹出而堵塞导管,装置A还需要做的一点改动是 。
(3)实验室用过氧化氢溶液制取氧气,应选择的发生装置是 ,反应的化学 方程式为 ,该反应的基本类型是 反应。若用C装置收集氧气,须等 时开始收集。
(4)实验室制取二氧化碳,常用的发生装置是 ,收集装置是 。若要收集到干燥的二氧化碳气体,应将发生装置与F装置的 (填“m”或“n”)端相连;F装置中的浓硫酸若换成 ,则可用来检验生成的二氧化碳。
.(10扬州27). (15分)叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究.
【应用研究】
(1)汽车经撞击后,30毫秒内引发NaN3,迅速分解为Na、N2,反应方程式为_______。
【制备研究】
(2)将金属钠与液态氨反应得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH3+N2O = NaN3+NaOH+X,实验室检验X气体使用的试纸是湿润________。
【Na2CO3质量分数测定】
工业级NaN3中常含有少量的Na2CO3,为测定样品中Na2CO3的质量分数设计如图
装置(已知H2SO4溶液与NaN3,反应不生成气体)。
(3)装置A的作用是_____。设计的实验步骤为:①精确称量样品,检查装置气密性;②打开弹簧夹,鼓入空气,称量装置C;③关闭弹簧夹,打开分液漏斗活塞;④再打开弹簧夹,_______;⑤再次称量装置C。计算碳酸钠含量至少需要测定______(填数字)个数据。根据制备反应,分析工业级NaN3中含有Na2CO3的可能原因_______。
【NaN3纯度测定】精确称量0.140 g NaN3样品,设计如图装置,测定其纯度。已知 (NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
(4)检查该装置气密性的方法是连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,两边高度差_____(填“变大”、“变小”或“不变”),说明气密性良好。
(5)使小试管中的NaN3样品与M溶液接触的操作是______。
(6)使用冷水冷凝的目的是______。反应前应将液面调节到量气管的“0”刻度,并使两边液面相平,反应后读数时,还需要进行的操作是_______。
(7)常温下测得量气管读数为67.2 mL(N2的密度为1.25 g/L),则实验中选用的量气管规格合适的是_____(填字母序号)。
A. 100 mL B. 1 L C. 2 L
(8)计算NaN3样品的纯度(写出计算过程)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com