
题目列表(包括答案和解析)
卤块的主要成分是MgCl2,此外还含 Fe3+、Fe2+ 和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如下图:
? 
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1表2提供的资料,填写空白:??
表1?? 生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
表2?? 化学试剂价格表
试剂 | 价格(元/吨) |
漂液(含NaClO,25.2%) | 450 |
双氧水(含H2O2 ,30%) | 2400 |
烧碱(含98% NaOH) | 2100 |
纯碱(含99.5% Na2CO3) | 600 |
(1)在步骤②中加入漂液而不是双氧水其原因是????????????????????????????????????????? 。
写出加入NaClO发生反应的离子方程式???????????????????????????????????????????????????????? 。
(2)在步骤③中控制pH=9.8,其目的是??????????????????????????????????????????????????????? 。
(3)沉淀物A的成分为????????????? ,试剂Z应该是?????????????? 。
(4)在步骤⑤中发生反应的化学方程式是?????????????????????????????????????????????????????? 。
(5)若在实验室中完成步骤⑥,则沉淀物必需在?????????? (填仪器名称)中灼烧。
(8分)卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。以卤块为原料制取轻质氧化镁的工艺流程如下:
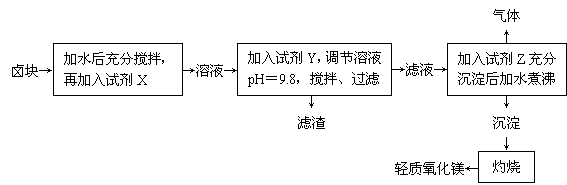
若要求产品中尽量不含有杂质,且生产成本较低,请根据下表中提供的资料,回答下列问题:
表1 生成氢氧化物沉淀的pH
物质 | 开始沉淀时的pH | 沉淀完全时的pH |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
Fe2+氢氧化物呈絮状,不易从溶液中除去,故常将它氧化成Fe3+,生成Fe(OH)3沉淀除去。
表2 原料价格表
物质 | 价格/元?吨-1 |
漂液(含25%NaClO) | 450 |
双氧水(含30%H2O2) | 2400 |
烧碱(含98%NaOH) | 2100 |
纯碱(含99.5%Na2CO3) | 600 |
⑴试剂X最好是 ,加入X的作用是 。
⑵调节pH=9.8的目的是 。
⑶加入试剂Z后发生的离子反应方程式为 。
⑷ 生产中产生的气体是CO2,写出产生CO2的化学方程式 。
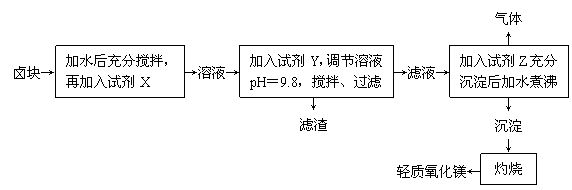 (8分)卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。以卤块为原料制取轻质氧化镁的工艺流程如下:
(8分)卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子。以卤块为原料制取轻质氧化镁的工艺流程如下:
若要求产品中尽量不含有杂质,且生产成本较低,请根据下表中提供的资料,回答下列问题:
表1 生成氢氧化物沉淀的pH
| 物质 | 开始沉淀时的pH | 沉淀完全时的pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6☆ |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
☆ Fe2+氢氧化物呈絮状,不易从溶液中除去,故常将它氧化成Fe3+,生成Fe(OH)3沉淀除去。
表2 原料价格表
| 物质 | 价格/元·吨-1 |
| 漂液(含25%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
⑴试剂X最好是 ▲ ,加入X的作用是 ▲ 。
⑵调节pH=9.8的目的是 ▲ 。
⑶加入试剂Z后发生的离子反应方程式为 ▲ 。
⑷ 生产中产生的气体是CO2,写出产生CO2的化学方程式 ▲ 。
“卤块”的主要成分为MgCl2(含Fe2+、Fe3+、Mn2+等杂质离子),若以它为原料,按如下工艺流程图,即可制得“轻质氧化镁”。如果要求产品尽量不含杂质离子,而且成本较低,流程中所用试剂或pH值控制可参考下列附表确定。轻质氧化镁工艺流程图如下:
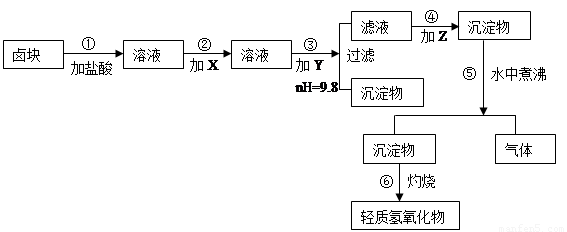
表1 化学试剂价格表
|
试剂 |
价格(元/ t ) |
|
漂液(含NaClO25.2%) H2O2(30%) NaOH(固98%) Na2CO3(固99.5%) 卤块(MgCl2,30%) |
450 2400 2100 600 310 |
表2 生成氢氧化物沉淀的值
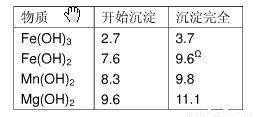
|
物质 |
开始沉淀 |
沉淀完全 |
|
Fe(OH)3 Fe(OH)2 Mn(OH)2 Mg(OH)2 |
2.7 7.6 8.3 9. |
3.7 9.6Ω 9.8 11.1 |
Ω注:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化成为Fe3+,生成Fe(OH)3沉淀而去除之。请填写以下空白:
⑴、在步骤②加入试剂X,最佳选择应是 ,其作用是 。
⑵、在步骤③加入的试剂Y应是 ,之所以要控制pH=9.8,其目的
是 。
⑶、在步骤⑤时发生的化学反应方程式是: 。
“卤块”的主要成分为MgCl2(含Fe2+、Fe3+、Mn2+等杂质离子),若以它为原料,按如下工艺流程图,即可制得“轻质氧化镁”。如果要求产品尽量不含杂质离子,而且成本较低,流程中所用试剂或PH值控制可参考下列附表确定

轻质氧化镁生产工艺流程图
表1 生成氢氧化物沉淀的PH值
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 Fe(OH)2 Mn(OH)2 Mg(OH)2 | 2.7 7.6 8.3 9.6 | 3.7 9.6 9.8 11.1 |
*)注:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常常将它氧化成为Fe3+,生成
Fe(OH)3沉淀而去除之。
表2 化学试剂价值表
| 试剂 | 价格(元/t) |
| 漂液(含NaClO25.2%) H2O2(30%) NaOH(固98%) Na2CO3(固99.5%) 卤块(MgCl2,30%) | 450 2400 2100 600 310 |
请填写以下空白:
(1)在步骤②加入的试剂X,最佳选择应是 ,其作用是 。
(2)步骤③加入的试剂Y应是 ;之所以要控制pH=9.8,其目的是 。
(3)在步骤⑤时发生的化学反应方程式是:
题号
1
2
3
4
5
6
7
8
答案
C
C
A
B
C
D
B
A
题号
9
10
11
12
13
14
15
16
答案
B
B
C
D
B
A
C
D

|