
题目列表(包括答案和解析)
向足量H2SO4溶液中加入100mL 0.4 mol?L―1 Ba(OH)2溶液,放出的热量是5.12kJ。如果向足量Ba(OH)2溶液中加入100mL 0.4mol?L―1 HCl溶液时,放出的热量为2.292kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式及中和热的有关叙述中正确的是( )
A.中和热△H=-57.3kJ?mol―1
B.稀的强酸与强碱反应的中和热为:△H=-128kJ?mol―1
C.Ba2+(aq)+SO42―(aq)=BaSO4(s);△H=-73kJ?mol―1
D.Ba2+(aq)+SO42―(aq)=BaSO4(s);△H=-13.4kJ?mol―1
向足量H2SO4溶液中加入100mL 0.4 mol?L―1 Ba(OH)2溶液,放出的热量是5.12kJ。如果向足量Ba(OH)2溶液中加入100mL 0.4 mol?L―1 HCl溶液时,放出的热量为2.2kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为:
A.Ba2+(aq)+SO42―(aq)=BaSO4(s) △H=-2.92kJ?mol―1
B.Ba2+(aq)+SO42―(aq)=BaSO4(s) △H=-0.72kJ?mol―1
C.Ba2+(aq)+SO42―(aq)=BaSO4(s) △H=-73kJ?mol―1
D.Ba2+(aq)+SO42―(aq)=BaSO4(s) △H=-18kJ?mol―1
化合物KxFe(C2O4)y?3H2O(Fe为+3价)是一种光敏材料,实验室可以用如下的方法来制备这种材料并测定这种材料的组成。
Ⅰ.制备
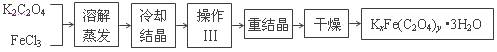
(1) 结晶时应将溶液用冰水冷却并在黑暗处等待晶体的析出,这样操作的原因是_______
_________________________________________________________。
(2)操作Ⅲ的名称是___________。
Ⅱ.组成测定
称取一定质量的晶体置于锥形瓶中,加入足量的蒸馏水和稀H2SO4,将C2O42-转化为H2C2O4后用0.1000 mol?L-1KMnO4溶液滴定,当消耗KMnO4溶液24.00mL时恰好完全反应;再向溶液中加入适量的还原剂,恰好将Fe3+完全转化为Fe2+,用KMnO4溶液继续滴定,当Fe2+完全氧化时,用去KMnO4溶液4.00mL。相关反应的化学方程式如下:
2 KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
(3)配制100mL 0.1000 mol?L-1KMnO4溶液及滴定实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒、锥形瓶外还有_______________________________(填仪器名称)。两个滴定中,终点时溶液颜色为________色,且30 秒内不变色。
(4)该化合物KxFe(C2O4)y?3H2O中,x=_______。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com