
题目列表(包括答案和解析)
太阳是银河系中极为普通的一颗恒星,剧烈的热核反应使之不断地向外辐射能量。太阳辐射的能量绝大部分集中在紫外波段,可见光波段和红外光波段,它们的能量分别占总辐射量的9%、44%和47%。地球的大气层中,基本不变的成分为氧、氮、氩等,占大气总量的99.96%,可变气体成分主要有CO2、水汽和臭氧等,这些气体的含量极小,但对大气物理状况的影响极大。大气臭氧层一般是指高度在离地面10~15Km的大气层,其中臭氧的浓度很低,将它折合成标准状况,其总累积厚度也不过0.3cm,其含量虽小,但对地球的气候和生物影响很大。
(1)大气压强P随距地面高度Z(m)的增大而减小,经验公式为PZ=![]() ,其中P0为地表的气压值,e=2.718。若臭氧层集中在24km的高空处,设在该高度处的温度为—50℃。试估算臭氧层的厚度。
,其中P0为地表的气压值,e=2.718。若臭氧层集中在24km的高空处,设在该高度处的温度为—50℃。试估算臭氧层的厚度。
(2)简要说明臭氧层对地球生物圈的意义。
![]() (3)臭氧层的生消可以简化成如下的反应方程:高层大气中的一个重要的光化学反应是氧分子吸收太阳辐射中波长λ<0.24μm的光子,离解为氧原子,即O2+hν(λ<0.24μm) O+O,由此可形成一系列的反应,其中最重要的是氧原子和氧分子在第三体(M)的参与下形成臭氧,其反应方程式为 。这里的M主要是氧分子或氮分子,它们是在反应过程中同时满足能量守恒和动量守恒所必须的。臭氧在λ<0.18μm的辐射作用下,能离解成氧分子和氧原子,其反应方程式为 。
(3)臭氧层的生消可以简化成如下的反应方程:高层大气中的一个重要的光化学反应是氧分子吸收太阳辐射中波长λ<0.24μm的光子,离解为氧原子,即O2+hν(λ<0.24μm) O+O,由此可形成一系列的反应,其中最重要的是氧原子和氧分子在第三体(M)的参与下形成臭氧,其反应方程式为 。这里的M主要是氧分子或氮分子,它们是在反应过程中同时满足能量守恒和动量守恒所必须的。臭氧在λ<0.18μm的辐射作用下,能离解成氧分子和氧原子,其反应方程式为 。
(4)人类的活动所产生的一些气体,能对大气中的臭氧起到破坏作用。使其含量减少,将造成严重后果,直接威胁到人类的生活和生存。近些年来,屡有在南极或北极,甚至在西藏出现臭氧空洞的报道,引起人们极大的关注。简要说明人类活动产生的那些气体对大气臭氧层能起破坏作用。
(16分)下图是一个化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH
2K2CO3+6H2O
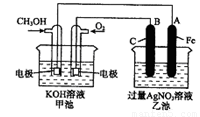
(1)请回答图中甲、乙两池的名称。甲电池是 装置,乙池是 装置。
(2)请回答下列电极的名称:通入CH3OH的电极名称是 ,B(石墨)电极的名称是 。
(3)写出电极反应式:
通入O2的电极的电极反应式是 。
A(Fe)电极的电极反应式为 ,
(4)乙池中反应的化学方程式为 。[来源:Z&xx&k.Com]
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下)
(10分)下表是元素周期表的一部分。表中所列字母分别代表一种化学元素。
|
a |
|
|
|||||||||||||||
|
b |
|
|
|
c |
d |
e |
f |
|
|||||||||
|
g |
h |
i |
j |
|
k |
l |
m |
||||||||||
|
n |
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
|
试回答下列问题:[来源:学*科*网Z*X*X*K]
(1)请写出元素O的基态原子电子排布式 。
(2)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填图中的序号),第一电离能最大的是 (填图中的序号)。

(3)由j原子跟c原子以1 : 1相互交替结合而形成的晶体,晶体类型与晶体j相同。两者相比熔点更高的是 (填化学式),试从结构角度加以解释 。
(4)COCl2俗称光气,分子中C原子采取 杂化成键;分子中的共价键含有 (填标号)
a.2个σ键 b.2个π键 c.1个σ键、2个π键 d.3个σ键、1个π键
X、Y、M、Z四种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素。下列说法不正确的是( )
A.化合物YZ3极易溶解于水
B.Z与M可以形成含18个电子的化合物
C.12g 14X中含有中子的物质的量为8mol
D.由上述四种元素组成的某盐可能受热易分解
【解析】地壳中含量最多的元素是氧,即M是O。X元素原子的最外层电子数是它的电子层数的2倍,则X是C或S,若是S,则根据X、Y、Z的电子层数之和为5,可知Y和Z的均属于第一周期,不正确,所以X只能是C。因为X、Y、M、Z四种短周期主族元素的原子半径依次减小,所以Z只能是氢元素。又因为Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,所以Y是N元素。A中是氨气,正确。B中是H2O2,正确。D中可以是NH4HCO3或(NH4)2CO3,正确。12g 14X中含有中子的物质的量为 ,所以答案是C。
,所以答案是C。
X、Y、M、Z四种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素。下列说法不正确的是( )
A.化合物YZ3极易溶解于水
B.Z与M可以形成含18个电子的化合物
C.12g 14X中含有中子的物质的量为8mol
D.由上述四种元素组成的某盐可能受热易分解
【解析】地壳中含量最多的元素是氧,即M是O。X元素原子的最外层电子数是它的电子层数的2倍,则X是C或S,若是S,则根据X、Y、Z的电子层数之和为5,可知Y和Z的均属于第一周期,不正确,所以X只能是C。因为X、Y、M、Z四种短周期主族元素的原子半径依次减小,所以Z只能是氢元素。又因为Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,所以Y是N元素。A中是氨气,正确。B中是H2O2,正确。D中可以是NH4HCO3或(NH4)2CO3,正确。12g 14X中含有中子的物质的量为![]() ,所以答案是C。
,所以答案是C。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com