
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)

 |
ƒ≥”–ª˙ŒÔAµƒœý∂‘∑÷◊”÷ ¡øŒ™94.5£¨‘⁄“ª∂®Ãıº˛œ¬ø…∑¢…˙»Áœ¬◊™ªØ(∆‰À˚≤˙ŒÔ∫ÕÀÆ“— °¬‘)£¨«Îªÿ¥œ¬¡–Œ £∫
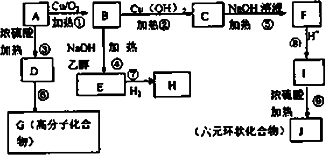
(1)∞¥“™«Û–¥ªØ—ß Ω£∫Aµƒ∑÷◊” Ω________JµƒΩ·ππºÚ Ω________£Æ
(2)‘⁄…œ ˆµƒ¢Ÿ£≠¢·∑¥”¶÷–£¨ Ù”⁄»°¥˙∑¥”¶µƒ «________£¨ Ù”⁄œ˚»•∑¥”¶µƒ «_________________£Æ
(3)–¥≥ˆœ¬¡–∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫B£≠C________C£≠F________£Æ
(4)”–ª˙ŒÔIø…∫œ≥…“ª÷÷ª∑±£–Õµƒ∏þ∑÷◊”≤ƒ¡œ£¨‘Ú∏þ∑÷◊”≤ƒ¡œµƒΩ·ππºÚ ΩŒ™_________________£Æ
(5)–¥≥ˆIµƒ“ª÷÷Õ¨∑÷“ÏππÃÂ(”ÎNa°¢NaOHµƒ“¯∞±»Ð“∫æ˘ƒÐ∑¥”¶)µƒΩ·ππºÚ Ω_________________£Æ







£®14∑÷£©∫œ≥…∆¯ «“‘H2°¢COµ»Œ™÷˜“™◊È≥…µƒπ©ªØ—ß∫œ≥…µƒ‘≠¡œ∆¯£¨ªÿ¥”–πÿŒ £∫
£®1£©º◊ÕÈ‘⁄“ª∂®Ãıº˛œ¬”ÎÀÆ∑¥”¶ø…µ√∫œ≥…∆¯£¨∏√∑¥”¶÷–√ø◊™“∆1£Æ2molµÁ◊”£¨À˘µ√∫œ≥…∆¯‘⁄±Ìøˆœ¬µƒÃª˝Œ™ L°£
£®2£©∫œ≥…∆¯‘⁄∫œ≥…∞±∆¯ ±–Ë≥˝»•CO£¨ø…¿˚”√“‘œ¬∑¥”¶£∫ CO£®g£©+H2O£®g£©![]() CO2£®g£©£´H2£®g£©
CO2£®g£©£´H2£®g£© ![]() H=-41£Æ16kJ£Ømol£¨∂‘”⁄∏√∑¥”¶”–πÿ±Ì ˆ’˝»∑µƒ « °£
H=-41£Æ16kJ£Ømol£¨∂‘”⁄∏√∑¥”¶”–πÿ±Ì ˆ’˝»∑µƒ « °£
a£Æ∆‰À˚Ãıº˛≤ª±‰£¨Àı–°ÃÂœµÃª˝‘ˆ¥Û—π«ø ±∑¥”¶ÀŸ¬ ≤ª±‰£¨À˘“‘∆Ω∫‚≤ª“∆∂Ø
b£Æ毻»Ãıº˛œ¬£¨»Ù≤‚µ√∏√ÃÂœµŒ¬∂»≤ª‘Ÿ∏ƒ±‰£¨‘Ú∑¥”¶¥¶”⁄∆Ω∫‚◊¥Ã¨
c£ÆŒ¬∂»…˝∏þ£¨∏√∑¥”¶∆Ω∫‚≥£ ˝‘ˆ¥Û
d£ÆŒ™Ã·∏þCO◊™ªØ¬ £¨ø… µ±‘ˆº”ÀÆ’Ù∆¯”√¡ø
ƒ≥Œ¬∂»œ¬£¨H2O∫ÕCO∞¥Ãª˝±»5£∫l≥‰»Îƒ≥∫„»ð∑¥”¶∆˜£¨∆Ω∫‚ ±≤‚µ√CO”ÎCO2ê˝±»l£∫9£¨‘Ú∏√Ãıº˛œ¬µƒ∆Ω∫‚≥£ ˝Œ™ £®±£¡Ù¡ΩŒª”––ß ˝◊÷£©
£®3£©Œ™≥˝»•£®2£©÷–…˙≥…µƒCO2£¨ø…”√úÀ·ºÿ»Ð“∫Œ¸ ’£¨≥£Œ¬œ¬pH=10µƒÃºÀ·ºÿ»Ð“∫÷–ÀƵÁ¿ÎµƒOH- µƒŒÔ÷ µƒ¡ø≈®∂»Œ™ £¨ÃºÀ·«‚ºÿ»Ð“∫÷–¿Î◊”≈®∂»¥Û–°À≥–ÚŒ™
£®4£©CO2∫ÕNH3‘⁄“ª∂®Ãıº˛œ¬∑¥”¶…˙≥…ƒÚÀÿ£€CO£®NH2£©2£ð£∫CO2£®g£©+2NH3£®1£©£ΩH2O£®1£©+CO£®NH2£©2£®1£©£¨CO2µƒ◊™ªØ¬ ÀÊŒ¬∂»±‰ªØ«˙œþ»Áœ¬£¨‘Ú∏√∑¥”¶![]() H 0£®ÃÓ°∞£æ°±ªÚ°∞£º°±£©£¨¥”∫œ≥…À˛ƒ⁄≥ˆ¿¥µƒ∆¯ÃÂ÷–»‘∫¨”–“ª∂®¡øµƒCO2°¢NH3£¨”¶»Á∫Œ¥¶¿Ì °£
H 0£®ÃÓ°∞£æ°±ªÚ°∞£º°±£©£¨¥”∫œ≥…À˛ƒ⁄≥ˆ¿¥µƒ∆¯ÃÂ÷–»‘∫¨”–“ª∂®¡øµƒCO2°¢NH3£¨”¶»Á∫Œ¥¶¿Ì °£
£®14∑÷£©∫œ≥…∆¯ «“‘H2°¢COµ»Œ™÷˜“™◊È≥…µƒπ©ªØ—ß∫œ≥…µƒ‘≠¡œ∆¯£¨ªÿ¥”–πÿŒ £∫
£®1£©º◊ÕÈ‘⁄“ª∂®Ãıº˛œ¬”ÎÀÆ∑¥”¶ø…µ√∫œ≥…∆¯£¨∏√∑¥”¶÷–√ø◊™“∆1£Æ2molµÁ◊”£¨À˘µ√∫œ≥…∆¯‘⁄±Ìøˆœ¬µƒÃª˝Œ™ L°£
£®2£©∫œ≥…∆¯‘⁄∫œ≥…∞±∆¯ ±–Ë≥˝»•CO£¨ø…¿˚”√“‘œ¬∑¥”¶£∫ CO£®g£©+H2O£®g£©![]() CO2£®g£©£´H2£®g£©
CO2£®g£©£´H2£®g£© ![]() H=-41£Æ16kJ£Ømol£¨∂‘”⁄∏√∑¥”¶”–πÿ±Ì ˆ’˝»∑µƒ « °£
H=-41£Æ16kJ£Ømol£¨∂‘”⁄∏√∑¥”¶”–πÿ±Ì ˆ’˝»∑µƒ « °£
a£Æ∆‰À˚Ãıº˛≤ª±‰£¨Àı–°ÃÂœµÃª˝‘ˆ¥Û—π«ø ±∑¥”¶ÀŸ¬ ≤ª±‰£¨À˘“‘∆Ω∫‚≤ª“∆∂Ø
b£Æ毻»Ãıº˛œ¬£¨»Ù≤‚µ√∏√ÃÂœµŒ¬∂»≤ª‘Ÿ∏ƒ±‰£¨‘Ú∑¥”¶¥¶”⁄∆Ω∫‚◊¥Ã¨
c£ÆŒ¬∂»…˝∏þ£¨∏√∑¥”¶∆Ω∫‚≥£ ˝‘ˆ¥Û
d£ÆŒ™Ã·∏þCO◊™ªØ¬ £¨ø… µ±‘ˆº”ÀÆ’Ù∆¯”√¡ø
ƒ≥Œ¬∂»œ¬£¨H2O∫ÕCO∞¥Ãª˝±»5£∫l≥‰»Îƒ≥∫„»ð∑¥”¶∆˜£¨∆Ω∫‚ ±≤‚µ√CO”ÎCO2ê˝±»l£∫9£¨‘Ú∏√Ãıº˛œ¬µƒ∆Ω∫‚≥£ ˝Œ™ £®±£¡Ù¡ΩŒª”––ß ˝◊÷£©
£®3£©Œ™≥˝»•£®2£©÷–…˙≥…µƒCO2£¨ø…”√úÀ·ºÿ»Ð“∫Œ¸ ’£¨≥£Œ¬œ¬pH=10µƒÃºÀ·ºÿ»Ð“∫÷–ÀƵÁ¿ÎµƒOH- µƒŒÔ÷ µƒ¡ø≈®∂»Œ™ £¨ÃºÀ·«‚ºÿ»Ð“∫÷–¿Î◊”≈®∂»¥Û–°À≥–ÚŒ™
£®4£©CO2∫ÕNH3‘⁄“ª∂®Ãıº˛œ¬∑¥”¶…˙≥…ƒÚÀÿ£€CO£®NH2£©2£ð£∫CO2£®g£©+2NH3£®1£©£ΩH2O£®1£©+CO£®NH2£©2£®1£©£¨CO2µƒ◊™ªØ¬ ÀÊŒ¬∂»±‰ªØ«˙œþ»Áœ¬£¨‘Ú∏√∑¥”¶![]() H 0£®ÃÓ°∞£æ°±ªÚ°∞£º°±£©£¨¥”∫œ≥…À˛ƒ⁄≥ˆ¿¥µƒ∆¯ÃÂ÷–»‘∫¨”–“ª∂®¡øµƒCO2°¢NH3£¨”¶»Á∫Œ¥¶¿Ì °£
H 0£®ÃÓ°∞£æ°±ªÚ°∞£º°±£©£¨¥”∫œ≥…À˛ƒ⁄≥ˆ¿¥µƒ∆¯ÃÂ÷–»‘∫¨”–“ª∂®¡øµƒCO2°¢NH3£¨”¶»Á∫Œ¥¶¿Ì °£
“ª°¢∂˛—°‘ÒÂ¥∞∏
1
2
3
4
5
6
B
D
D
A
C
C
7
8
9
10
11
12
A
C
D
C
D
C
13
14
15
16
17
18
B
C
D
A
D
D
19
20
21
22
23
D
B
C
B
A
»˝°¢
24°¢£®7∑÷£©
(1) H £∫ O £∫ H (1∑÷)
£®2∑÷£©3NO2+H2O=2HNO3+NO
Cl2+H2O=HCl+HClO
2Na2O2+2H2O=4NaOH+O2°¸
25°¢£®6∑÷£©
£®1£© C —ı‘≠◊”Ω·ππ æ“‚Õº £®√øø’1∑÷£©
 £®2£©
Al2(SO4)3 £®1∑÷£© Al3+ +
3H2O
Al(OH)3 +3 H+ £®2∑÷£© ¡ÚÀ·ªÚ—«¡ÚÀ·ªÚúÀ·£®1∑÷£©£®–¥≥ˆ“ª÷÷º¥ø…£¨∫œ¿Ì¥∞∏“≤ø…£©
£®2£©
Al2(SO4)3 £®1∑÷£© Al3+ +
3H2O
Al(OH)3 +3 H+ £®2∑÷£© ¡ÚÀ·ªÚ—«¡ÚÀ·ªÚúÀ·£®1∑÷£©£®–¥≥ˆ“ª÷÷º¥ø…£¨∫œ¿Ì¥∞∏“≤ø…£©
26°¢£®8∑÷£©
£®1£©ºŸ…Ë2£∫»Ð“∫÷–¥Ê‘⁄HCO3-
ºŸ…Ë3£∫»Ð“∫÷–¥Ê‘⁄CO32-∫ÕHCO3-
ºŸ…Ë4£∫»Ð“∫÷–¥Ê‘⁄CO32-∫ÕSO42-
ºŸ…Ë5£∫»Ð“∫÷–¥Ê‘⁄SO42 °¢HCO3- £®À≥–Ú≤ªœÞ°££©£®∏˜1∑÷£©
£®2£©¢Ÿ”√Ω∫Õ∑µŒπл°…Ÿ¡ø»Ð“∫º”»Î ‘πÐ÷–£¨‘Ÿ”√µŒπл°π˝¡øµƒ1mol/L¬»ªØ±µ»Ð“∫≤¢µŒº”µΩ ‘πÐA÷–£¨≥‰∑÷∑¥”¶∫Û£¨æ≤÷√£¨»ª∫Ûπ˝¬À£¨Ω´≥¡µÌ∫Õ¬À“∫∑÷±◊∞»Î¡ÌÕ‚µƒ¡Ω∏ˆ ‘πÐ÷–£®2∑÷£©£ª≤˙…˙∞◊…´≥¡µÌ°£
¢⁄Õ˘◊∞”–≥¡µÌµƒ ‘πÐ÷–º”»Îπ˝¡øµƒ2mol/L—ŒÀ·£ª≥¡µÌ≤ø∑÷»ÐΩ‚«“”–∆¯ÃÂ…˙≥…°£Àµ√˜‘≠»Ð“∫÷–“ª∂®∫¨”–SO42-∫ÕCO32-°£
¢€Õ˘◊∞”–¬À“∫µƒ ‘πÐ÷–º”»Î2mol/L—ŒÀ·£ª≥ˆœ÷ŒÞ…´∆¯Ã£¨Àµ√˜‘≠»Ð“∫÷–∫¨”–HCO3-°£
£®£®√øø’∏˜1∑÷°£∆‰À˚∫œ¿Ì∑Ω∞∏≤Œ’’∏¯∑÷£©
27°¢£®13∑÷£©£®1£©≤ªƒÐ £®1∑÷£© Œ¬∂»∏þ£¨ÀÆŒ™∆¯Ã¨,≤ª¿˚”⁄∞±∆¯µƒ…˙≥… £®2∑÷£©
(2) 25% £®2∑÷£©K= £®1∑÷£© ºı–° ºı–° £®2∑÷£©
(3) C3H3N6 £®2∑÷£©6CO(NH2)2=6NH3+3CO2+C3H6N6 £®2∑÷£©
N C N H H £®1∑÷£©
28°¢£®10∑÷£©
(1) µ⁄Àƒ÷Ð∆⁄£¨µ⁄¢¯◊ £®2∑÷£©
(2) 3Fe3O4+8Al=9Fe+4Al2O3 £®2∑÷£© ”…¿¥“±¡∂ƒ—»€Ω Ù£®∆‰À˚’˝»∑¥∞∏≤Œ’’∏¯∑÷£©£®1∑÷£©
Al2O3+2OH-=2AlO2-+H2O £®2∑÷£©
(3) Cl2+2Fe2+=2Fe3++2Cl- £®1∑÷£© 3SCN-+Fe3+=Fe£®SCN£©3 £®2∑÷£©
29°¢£®15∑÷£©
¢≈¢Ÿ—Ù¿Î◊”Ωªªªƒ§ £®2∑÷£© ¢⁄ 2Cu2++4e-=2Cu 4OH-®D4e-=2H2O+O2 £®∏˜1∑÷£©
£®2£©Cl2+2Br-=Br2+2Cl- £®2∑÷£© BrO3- 5Br- £®∏˜1∑÷£©
∑÷“∫¬©∂∑ …’±≠£®∏˜1∑÷£© ¢⁄ £®1∑÷£©
£®3£©H2S+HDO=HDS+H2O ¢€H2S£®√øø’2∑÷£¨π≤10∑÷£©
30°¢£®15∑÷£©
£®1£©B (1∑÷) µ⁄4÷Ð∆⁄µ⁄IB◊ £®∏˜1∑÷£© 1s22s22P63s23P63d104s1ªÚ[Ar] 3d104s1 (2∑÷) (2) CO2 °¢CCl4 £®∆‰À˚∫œ¿Ì¥∞∏≤Œ’’∏¯∑÷£©(∏˜1∑÷) ∑÷◊”æßà‘≠◊”æßà(∏˜1∑÷) £®3£© 7 1 £®∏˜1∑÷£© £®4£© IIIA IVA £ª b (∏˜1∑÷)
Aµ„À˘ 浃«‚ªØŒÔ «ÀÆ£¨∆‰∑–µ„‘⁄—ı◊‘™Àÿµƒ«‚ªØŒÔ÷–◊Ó∏þ «”…”⁄‘⁄ÀÆ∑÷◊”º‰¥Ê‘⁄◊≈«‚º¸£¨∆‰«ø∂»‘∂¥Û”⁄∑÷◊”º‰◊˜”√¡¶°££®1∑÷£©
31°¢£®15∑÷£©¬‘
(1) £®∏˜1∑÷£©
(2) £®∏˜1∑÷£©
£®3£© £®∏˜2∑÷£©
(4) 3 3:2:2 £®∏˜1∑÷£©
£®5£© £®∏˜1∑÷£©

 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com