
题目列表(包括答案和解析)

 ” 为铜片):
” 为铜片): 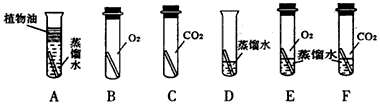
(09玉林、防城港)2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见右图),发表严正声明:中国对其拥有不可置疑的所有权。目前我国正在积极追讨这两件文物。兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿)。为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:
1.探究铜绿的组成
【查阅资料】 通过查阅资料知道:铜绿受热易分解。
【设计与实验】
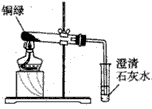
(1)小芳从其它铜器上取下适量的干燥铜绿,按右图所示装置进行实验。在实验过程中,观察到:试管口内有水珠出现,说明了铜绿中含有氢、氧元素;澄清石灰水变浑浊,说明了铜绿中含有 元素。
(2)小芳取下少量试管内反应后的剩余物,放入另一支试管中,滴人稀硫酸,充分反应后,溶液变蓝色,说明铜绿中含有 元素。
【实验结论】 铜绿是由铜、氢、氧和碳元素组成的。
2.探究铜生成铜绿的条件
【查阅资料】铜绿的化学式是Cu2(OH)2CO3,它受热会分解生成三种氧化物。铜绿分解的化学方程式为 。
【猜想与假设】 据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及 共同作用而形成的。
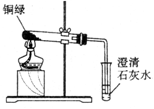
【设计与实验】 借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮,试管内的“ ”为铜片):
实验较长时间后,发现 试管中铜片最先生锈(填试管字母编号)。
【评价与改进】 小区认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是(用图表示亦可) 。
【拓展与应用】
小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?请你说明理由。
。
(09玉林、防城港)2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见右图),发表严正声明:中国对其拥有不可置疑的所有权。目前我国正在积极追讨这两件文物。兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿)。为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:
1.探究铜绿的组成
【查阅资料】 通过查阅资料知道:铜绿受热易分解。
【设计与实验】
(1)小芳从其它铜器上取下适量的干燥铜绿,按右图所示装置进行实验。在实验过程中,观察到:试管口内有水珠出现,说明了铜绿中含有氢、氧元素;澄清石灰水变浑浊,说明了铜绿中含有 元素。
(2)小芳取下少量试管内反应后的剩余物,放入另一支试管中,滴人稀硫酸,充分反应后,溶液变蓝色,说明铜绿中含有 元素。
【实验结论】 铜绿是由铜、氢、氧和碳元素组成的。
2.探究铜生成铜绿的条件
【查阅资料】铜绿的化学式是Cu2(OH)2CO3,它受热会分解生成三种氧化物。铜绿分解的化学方程式为 。
【猜想与假设】 据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及 共同作用而形成的。
【设计与实验】 借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮,试管内的“ ”为铜片):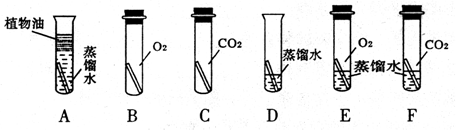
实验较长时间后,发现 试管中铜片最先生锈(填试管字母编号)。
【评价与改进】 小区认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是(用图表示亦可) 。
【拓展与应用】
小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?请你说明理由。
。
(09玉林、防城港)2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见右图),发表严正声明:中国对其拥有不可置疑的所有权。目前我国正在积极追讨这两件文物。兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿)。为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:


1.探究铜绿的组成
【查阅资料】 通过查阅资料知道:铜绿受热易分解。
【设计与实验】
(1)小芳从其它铜器上取下适量的干燥铜绿,按右图所示装置进行实验。在实验过程中,观察到:试管口内有水珠出现,说明了铜绿中含有氢、氧元素;澄清石灰水变浑浊,说明了铜绿中含有 元素。
(2)小芳取下少量试管内反应后的剩余物,放入另一支试管中,滴人稀硫酸,充分反应后,溶液变蓝色,说明铜绿中含有 元素。
【实验结论】 铜绿是由铜、氢、氧和碳元素组成的。
2.探究铜生成铜绿的条件
【查阅资料】铜绿的化学式是Cu2(OH)2CO3,它受热会分解生成三种氧化物。铜绿分解的化学方程式为 。
【猜想与假设】 据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及 共同作用而形成的。
【设计与实验】 借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮,试管内的“ ”为铜片):

实验较长时间后,发现 试管中铜片最先生锈(填试管字母编号)。
【评价与改进】 小区认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验。你认为要补充的一个实验是(用图表示亦可) 。
【拓展与应用】
小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿比青铜器的少,他据此分析认为青铜比纯铜易锈蚀。小明的分析是否全面?请你说明理由。
。
一、选择题(每小题1分,共30分)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
A
C
C
C
D
D
C
A
B
题号
11
12
13
14
15
16
17
18
19
20
答案
B
B
D
C
D
C
C
B
B
D
题号
21
22
23
24
25
26
27
28
29
30
答案
A
D
C
C
A
C
C
A
A
A
二、填空题(每空1分,共26分)
31.(7分)(1) Fe2O3+3CO高温 2Fe+3CO2 ; (12 + 1×2 +19×2) ×n
(2) ① B 、D 、E ; ② A ; ③ 隔绝空气做保护气
(3)① A ; ② A
 32.(6分)(1)物理变化
32.(6分)(1)物理变化
(2)① CH4 + 2O2 CO2 + 2H2O
②A、B、C、D
 (3)① 玻璃棒
(3)① 玻璃棒
 ② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
③ Na2CO3 + 2HCl 2NaCl + H2O + CO2 ↑
33.(4分) ① 6:7:2:1
② 防食品被氧化和挤压破碎
③ 铁粉
④ 相同条件时,气体分子比液态物质分子运动的快

 34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
② 2H2O 2H2O + O2 ↑
 ③ CaO + H2O Ca(OH)2
③ CaO + H2O Ca(OH)2
 ④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
(2) NH4NO3
35.(4分)(1) CO2
(2) 纯碱

 (3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(4) Ca(OH)2 + Na2CO3 CaCO3↓+ 2NaOH
三、实验题(共18分)
 36. (6分)(1) ①试管 ②锥形瓶
36. (6分)(1) ①试管 ②锥形瓶
(2)A、B ;D、F ;2KMnO4 K2MnO4 + MnO2 + O2 ↑
(3)B、D
37. (6分)【查阅资料】①
请你完成下表中空余部分。
猜想
实验设计及装置
观察到的实验现象
猜想②
果肉表面出现咖啡色
猜想④
果肉表面未出现咖啡色
猜想⑤
B、F
【反思与评价】氧气溶于水,会慢慢氧化果肉。
【应用】使用保护气和煮沸过的凉水,保存时加保护气或抽出空气且密闭。
38.(6分) (1)填充实验过程空格项:
实 验 步 骤
实 验 现 象
实 验 结 论
步骤①
溶液变红 。

步骤②
边加边搅拌 。
步骤③


步骤④
有无色晶体析出 。
浓硫酸有吸水性。
(3)总结:A. H+ 、OH-
B. 25%
四、计算题(共6分)
 39. (1)解:设样品未被氧化的镁的质量为X
39. (1)解:设样品未被氧化的镁的质量为X
Mg + H2SO4 = MgSO4 + H2 ↑
24 2 (1分)
X
24:2 = X:
(2)解:样品MgO的质量=

 样品被氧化前的质量=
样品被氧化前的质量=
答: 略 (1分)
40.(1) 2.8 (1分)
(2) 82.5% (1分)
(3)由试题分析20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应
解:设盐酸溶液中溶质的质量分数为x。
CaCO3 + 2HCl =CaCl2+H2O+CO2↑
100 73
100∶73 =
x=18.25% (1分)
房山区2008学年初三化学第二次统测试卷参考答案
一、选择题(每小题1分,共30分)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
A
C
C
C
D
D
C
A
B
题号
11
12
13
14
15
16
17
18
19
20
答案
B
B
D
C
D
C
C
B
B
D
题号
21
22
23
24
25
26
27
28
29
30
答案
A
D
C
C
A
C
C
A
A
A
二、填空题(每空1分,共26分)
31.(7分)(1) Fe2O3+3CO高温 2Fe+3CO2 ; (12 + 1×2 +19×2) ×n
(2) ① B 、D 、E ; ② A ; ③ 隔绝空气做保护气
(3)① A ; ② A
 32.(6分)(1)物理变化
32.(6分)(1)物理变化
(2)① CH4 + 2O2 CO2 + 2H2O
②A、B、C、D
 (3)① 玻璃棒
(3)① 玻璃棒
 ② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
③ Na2CO3 + 2HCl 2NaCl + H2O + CO2 ↑
33.(4分) ① 6:7:2:1
② 防食品被氧化和挤压破碎
③ 铁粉
④ 相同条件时,气体分子比液态物质分子运动的快

 34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
② 2H2O 2H2O + O2 ↑
 ③ CaO + H2O Ca(OH)2
③ CaO + H2O Ca(OH)2
 ④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
(2) NH4NO3
35.(4分)(1) CO2
(2) 纯碱

 (3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(4) Ca(OH)2 + Na2CO3 CaCO3↓+ 2NaOH
三、实验题(共18分)
 36. (6分)(1) ①试管 ②锥形瓶
36. (6分)(1) ①试管 ②锥形瓶
(2)A、B ;D、F ;2KMnO4 K2MnO4 + MnO2 + O2 ↑
(3)B、D
37. (6分)【查阅资料】①
请你完成下表中空余部分。
猜想
实验设计及装置
观察到的实验现象
猜想②
果肉表面出现咖啡色
猜想④
果肉表面未出现咖啡色
猜想⑤
B、F
【反思与评价】氧气溶于水,会慢慢氧化果肉。
【应用】使用保护气和煮沸过的凉水,保存时加保护气或抽出空气且密闭。
38.(6分) (1)填充实验过程空格项:
实 验 步 骤
实 验 现 象
实 验 结 论
步骤①
溶液变红 。

步骤②
边加边搅拌 。
步骤③


步骤④
有无色晶体析出 。
浓硫酸有吸水性。
(3)总结:A. H+ 、OH-
B. 25%
四、计算题(共6分)
 39. (1)解:设样品未被氧化的镁的质量为X
39. (1)解:设样品未被氧化的镁的质量为X
Mg + H2SO4 = MgSO4 + H2 ↑
24 2 (1分)
X
24:2 = X:
(2)解:样品MgO的质量=

 样品被氧化前的质量=
样品被氧化前的质量=
答: 略 (1分)
40.(1) 2.8 (1分)
(2) 82.5% (1分)
(3)由试题分析20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应
解:设盐酸溶液中溶质的质量分数为x。
CaCO3 + 2HCl =CaCl2+H2O+CO2↑
100 73
100∶73 =
x=18.25% (1分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com