
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
½«22.4gĶŗĶŃõ»ÆĢśµÄ»ģŗĻĪļ·ŪÄ©¼ÓČėµ½ÅضČĪŖ1mol/LµÄĮņĖįÖŠ£¬¹ĢĢåĒ”ŗĆĶźČ«Čܽā£¬µĪČėKSCNČÜŅŗ²»ĻŌÉ«£¬“ĖŹ±ĻūŗÄĮņĖįĢå»żĪŖVL”£
£Ø1£©ĮņĖįĢå»żVµÄ L”£
£Ø2£©½«ĖłµĆČÜŅŗŹĶŹĶµ½1L£¬Ēó“ĖŹ±ČÜŅŗÖŠ½šŹōŃōĄė×ÓĪļÖŹµÄĮæÅØ¶Č£æ
½«22.4gĶŗĶŃõ»ÆĢśµÄ»ģŗĻĪļ·ŪÄ©¼ÓČėµ½ÅضČĪŖ1 mol•L-1µÄĮņĖįÖŠ£¬Ź¹Ö®·¢Éś·“Ó¦”£
¢ÅČō¹ĢĢåĒ”ŗĆČ«²æČܽā£¬ĻūŗÄĮņĖįµÄĢå»żĪŖV L £¬ĒóVµÄȔֵ·¶Ī§”£
¢ĘČōĮņĖįČÜŅŗ¹żĮ棬·“Ó¦ŗóČÜŅŗµÄĢå»żĪŖ1 L£¬²āµĆ“ĖČÜŅŗÖŠFe2+ÅضČĪŖ0.1 mol•L-1£¬ĒóŌ»ģŗĻĪļŗ¬Ķ¶ąÉŁæĖ”£
¢ÅČō¹ĢĢåĒ”ŗĆČ«²æČܽā£¬ĻūŗÄĮņĖįµÄĢå»żĪŖV L £¬ĒóVµÄȔֵ·¶Ī§”£
¢ĘČōĮņĖįČÜŅŗ¹żĮ棬·“Ó¦ŗóČÜŅŗµÄĢå»żĪŖ1 L£¬²āµĆ“ĖČÜŅŗÖŠFe2+ÅضČĪŖ0.1 mol•L-1£¬ĒóŌ»ģŗĻĪļŗ¬Ķ¶ąÉŁæĖ”£
³£ĪĀĻĀ£¬·“Ó¦
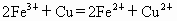 ŌŚĖ®ČÜŅŗÖŠÄÜ·¢Éś£¬½«22.4gĶŗĶČżŃõ»Æ¶žĢśµÄ»ģŗĻ·ŪÄ©¼ÓČėµ½ÅضČĪŖ1mol/LµÄĮņĖįÖŠ£¬Ź¹Ö®·¢Éś·“Ó¦£®
ŌŚĖ®ČÜŅŗÖŠÄÜ·¢Éś£¬½«22.4gĶŗĶČżŃõ»Æ¶žĢśµÄ»ģŗĻ·ŪÄ©¼ÓČėµ½ÅضČĪŖ1mol/LµÄĮņĖįÖŠ£¬Ź¹Ö®·¢Éś·“Ó¦£®
(1)Čō¹ĢĢåĒ”ŗĆČ«²æČܽā£¬ĻūŗÄĮņĖįµÄĢå»żĪŖVL£¬ĒóVµÄȔֵ·¶Ī§£®
(2)ČōĮņĖįČÜŅŗ¹żĮ棬·“Ó¦ŗóČÜŅŗµÄĢå»żĪŖ1L£¬²āµĆ“ĖČÜŅŗÖŠ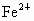 µÄÅضČĪŖ0.1mol/L£¬ĒóŌ»ģŗĻĪļÖŠŗ¬Ķ¶ąÉŁæĖ?
µÄÅضČĪŖ0.1mol/L£¬ĒóŌ»ģŗĻĪļÖŠŗ¬Ķ¶ąÉŁæĖ?
³£ĪĀĻĀ£¬·“Ó¦
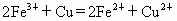 ŌŚĖ®ČÜŅŗÖŠÄÜ·¢Éś£¬½«22.4gĶŗĶČżŃõ»Æ¶žĢśµÄ»ģŗĻ·ŪÄ©¼ÓČėµ½ÅضČĪŖ1mol/LµÄĮņĖįÖŠ£¬Ź¹Ö®·¢Éś·“Ó¦£®
ŌŚĖ®ČÜŅŗÖŠÄÜ·¢Éś£¬½«22.4gĶŗĶČżŃõ»Æ¶žĢśµÄ»ģŗĻ·ŪÄ©¼ÓČėµ½ÅضČĪŖ1mol/LµÄĮņĖįÖŠ£¬Ź¹Ö®·¢Éś·“Ó¦£®
(1)Čō¹ĢĢåĒ”ŗĆČ«²æČܽā£¬ĻūŗÄĮņĖįµÄĢå»żĪŖVL£¬ĒóVµÄȔֵ·¶Ī§£®
(2)ČōĮņĖįČÜŅŗ¹żĮ棬·“Ó¦ŗóČÜŅŗµÄĢå»żĪŖ1L£¬²āµĆ“ĖČÜŅŗÖŠ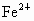 µÄÅضČĪŖ0.1mol/L£¬ĒóŌ»ģŗĻĪļÖŠŗ¬Ķ¶ąÉŁæĖ?
µÄÅضČĪŖ0.1mol/L£¬ĒóŌ»ģŗĻĪļÖŠŗ¬Ķ¶ąÉŁæĖ?
Ņ»”¢£Ø¹²44·Ö£¬Ć抔Ģā2·Ö£©
ĢāŗÅ
1
2
3
4
5
6
7
8
9
10
11
“š°ø
B
C
B
D
B
C
C
A
B
D
A
ĢāŗÅ
12
13
14
15
16
17
18
19
20
21
22
“š°ø
A
A
C
A
D
C
A
D
B
C
B
¶ž”¢£Ø±¾Ģā°üĄØ3Š”Ģā£¬¹²22·Ö£©
23£®£Ø¹²8·Ö£¬ĆææÕ2·Ö£©
¢ÅĪŽ””””””””¢ĘNO2£»H2O”¢AgNO3ČÜŅŗ£ØĘäĖüŗĻĄķ“š°ø¾łøų·Ö£©
¢ĒH2(g)£«1/2O2(g) H2O(l)£»”÷H=£285.8kJ?mol£1
H2O(l)£»”÷H=£285.8kJ?mol£1
24.£Ø¹²10·Ö£¬ĆææÕ2·Ö£©
¢Å2Al£«2OH££«2H2O===2AlO2££«3H2”ü£»²»ÄÜ
¢Ę £»2NaHCO3
£»2NaHCO3 Na2CO3£«H2O£«CO2”ü””””””¢ĒČż½Ē׶ŠĪ
Na2CO3£«H2O£«CO2”ü””””””¢ĒČż½Ē׶ŠĪ
25.£Ø¹²4·Ö£¬ĆææÕ2·Ö£©
¢ÅN””””””””¢Ę·Ē¼«ŠŌ
Čż”¢£Ø±¾Ģā°üĄØ2Š”Ģā£¬¹²12·Ö£©
26.£Ø¹²4·Ö£¬ĆææÕ2·Ö£©
¢Å·ÖŅŗĀ©¶·””””””¢ĘNaOH¹ĢĢå»ņ¼īŹÆ»Ņ
27£®£Ø¹²8·Ö£¬ĆææÕ2·Ö£©
¢Åb””””””¢ĘÅØĮņĖį””””””””(3)¢Ś¢Ū¢Ł¢Ż¢Ü(»ņ¢Ū¢Ś¢Ł¢Ż¢Ü)
(4)ĪüŹÕ¶ąÓąCl2£¬·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČė·“Ó¦Ó¦Ę÷Ź¹S2Cl2Ė®½ā
ĖÄ”¢£Ø±¾Ģā°üĄØ2Š”Ģā£¬¹²12·Ö£©
28.£Ø¹²4·Ö£¬ĆææÕ2·Ö£©
¢ÅÄÜ””””””””””¢Ę3
29.£Ø¹²8·Ö£¬ĆææÕ2·Ö£©
¢ÅōĒ»ł””””””””””¢ĘĻūČ„·“Ó¦””””
¢Ē ””””¢Č
””””¢Č
Ī唢£Ø±¾Ģā°üĄØ2Š”Ģā£¬¹²10·Ö£©
30.£Ø¹²6·Ö£©v(H2SO4)=200mL£»c(Cu2£«)=0.5mol?L£1
31.£Ø¹²4·Ö,ĆææÕ2·Ö£©
¢Å94.6%””””””””¢Ę13
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com